|
|
|
高中化学知识点总结《热化学方程式》试题预测(2020年最新版)(五)
2020-08-23 06:22:48
【 大 中 小】
|
1、选择题 下列热化学方程式中的反应热又为燃烧热的是 ( )
A.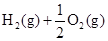
|
2、选择题 已知:
CH3CH2CH2CH3(g) +6.5O2(g)=4CO2(g) +5H2O(l) △H=-2878kJ/mol
(CH3)2CHCH3(g)+6.5O2(g)=4CO2(g)+5H2O(l) △H=-2869kJ/mol
下列说法正确的是
[? ]
A.正丁烷分子储存的能量大于异丁烷分子
B.正丁烷的稳定性大于异丁烷
C.异丁烷转化为正丁烷的过程是一个放热过程
D.异丁烷分子中的碳氢键比正丁烷的多
3、填空题 (15分)在火箭推进器中装有强还原剂肼(N2H4)和强氧化剂过氧化氢,当它们混合时,即产生大量氮气和水蒸气,并放出大量热。已知0.4mol液态肼与足量过氧化氢反应,生成氮气和水蒸气,放出256.65kJ的热量。
(1)写出肼和过氧化氢的结构式。肼__________________,过氧化氢______________ 。
(2)写出热化学方程式_________________________________________________。
(3)已知H2O(1)==H2O(g) △H=+44kJ/mol,则16g液态肼与足量液态过氧化氢反应生成氮气和液态水时,放出的热量是_____________________ kJ。
(4)上述反应用于火箭推进剂,除释放大量热和快速产生大量气体外,还有一个很突出的优点是________________________________________________________。
4、填空题 (16分)
I.制取三氧化硫反应的化学方程式为:2SO2(g)十O2(g) 2SO3(g) 2SO3(g)
(1)此反应是工业上生产 的重要步骤。
(2)能够说明在恒温恒容条件下,上述反应已经达到化学平衡状态的是 (填序号).
a.每生成1mol SO3的同时生成0.5mol O2
b.容器中混合气体的密度不变
c.SO2、O2、SO3的物质的量之比为2:1:2
d.容器中气体总压强不变
(3)在400℃时,常压下,容积为1.0L的密闭容器中充入1.00mol SO2(g)和0.96mol O2(g),充分反应后,测得还有0.04mol SO2剩余,并放出190.08KJ的热量。
①根据有关数据,请分析在工业生产中选择常压反应器的原因:
。
②写出此反应的热化学方程式:
2SO2(g)十O2(g) 2SO3(g) △H= 。 2SO3(g) △H= 。
Ⅱ.(1)在某温度下,把1.00 mol NH3溶于水中配成1.00 L溶液,测得溶液中OH-浓度和时间的图像如下:
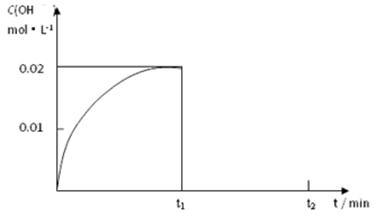
①求该温度时,氨水的电离平衡常数K= 。
② 在t1时刻再加入H2O配成2L溶液,于t2时刻重新达到平衡,请在坐标系中画出t1~t2时间内OH-浓度随时间变化的曲线。
(2)将a mol/L的盐酸和b mol/L氨水等体积混合,混合后体积为混合前体积之和,充分反应后所得溶液显中性。
① a b (填“<”、“=”或“>”)
② 根据物料守恒原理,求混合后溶液中剩余氨水浓度:c(NH3・H2O)= 。
(用含有a、b的式子表示)
5、填空题 已知下列反应的平衡常数:
(1)HCN H+ + CN-, K(1)Θ =" 4.9" ×10-10 H+ + CN-, K(1)Θ =" 4.9" ×10-10
(2)NH3 + H2O  NH4+ + OH-, K(2)Θ =" 1.8" ×10-5 NH4+ + OH-, K(2)Θ =" 1.8" ×10-5
(3)H2O H+ + OH-, KwΘ =" 1.0" ×10-14算出NH3 + HCN H+ + OH-, KwΘ =" 1.0" ×10-14算出NH3 + HCN  NH4+ + CN-, 反应平衡常数的K值是_________________ NH4+ + CN-, 反应平衡常数的K值是_________________
|