1、选择题 下列物质的成分或主要成分相同的是
A.金刚石和石墨
B.冰和干冰
C.小苏打和烧碱
D.钢铁和煤
参考答案:A
本题解析:A项两物质化学成分为碳;B项干冰的化学成分为二氧化碳;C项小苏打的化学成分为NaHCO3,烧碱为NaOH;D项钢铁是铁的合金,煤是有机物和无机物的混合物.
本题难度:一般
2、填空题 (8分)由A、B元素组成的含4个原子核共42个电子的负二价阴离子中,每1个A的核内质子数比B的核内质子数多8个,试通过计算确定:
(1)A、B元素名称分别为____________和___________。
(2)写出该阴离子的离子符号________________。
(3)该阴离子与钠离子形成的化合物中含有__________键。
参考答案:(每空2分,共8分)
(1)硫,氧;(2)SO32--;(3)离子键、共价键
本题解析:设阴离子中含x个A原子,其质子数为a+8,则含有4-x个B原子,其质子数为a;
则x×(a+8)+ (4-x)×a +2 =42,可求得当x=1时,a=8符合题意,则可知两元素分别为:S、O
本题难度:简单
3、选择题 关于下列图示的说法中正确的是
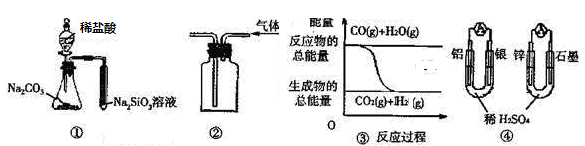
A.用图 ① 所示实验可比较氯、碳、硅三种元素的非金属性强弱
B.用图 ② 所示实验装置排空气法收集CO2气体

C.图 ③ 表示反应 CO(g)+H2O(g) CO2(g)+H2(g)是放热反应
D.图 ④ 两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同
参考答案:C
本题解析:A、不能用盐酸,且盐酸易挥发,应用元素最高价氧化物的水化物比较酸性强弱,即此装置不能证明氯、碳、硅三种元素非金属性的强弱,故A错误;B、收集CO2应用向上排空气法,进气管应插入到集气瓶底部,故B错误;C、反应物总能量大于生成物总能量,应为放热反应,故C正确;D、两装置的负极反应分别为Al-3e-=Al3+、Zn-2e-=Zn2+,故通过导线的电子数相同时,消耗负极材料的物质的量不相同,D错误。
本题难度:简单
4、填空题 (9分)A、X、Y、Z和W是原子序数依次增大的五种短周期元素。A和X可组成两种常温下为液态的化合物A2X、A2X2,X和Y也可组成两种常温下为固态的化合物Y2X、Y2X2,且Y2X、Y2X2的焰色反应均为黄色。在元素周期表中,A与Y同主族,X与Z同主族,Z与W相邻。请同答:
(1)A2X2的结构式?,Y2X2的电子式?。
(2)X、Z两种元素的氢化物中熔沸点较高的是?(填化学式,下同);工业上将Z的低价氧化物转化为高价氧化物的化学方程式为?。
(3)W元素在周期表中的位置为?;实验室制备W单质的化学反应方程式为?;在上述反应中氧化剂和还原剂的物质的量比为?。
参考答案:(1)H-O-O-H;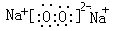
(2)H2O? 2SO2+O2 2SO3
2SO3
(3)第三周期第VIIA族? 4HCl(浓)+MnO2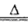 2H2O + Cl2↑+MnCl2;1:2
2H2O + Cl2↑+MnCl2;1:2
本题解析:(1)A和X可组成两种常温下为液态的化合物A2X、A2X2,可判断A是H元素,X是O元素;O与Na也可组成两种常温下为固态的化合物Y2X、Y2X2,且Y2X、Y2X2的焰色反应均为黄色,所以Y是Na;则Z是S元素,W是Cl元素。
(1)A2X2的结构式即过氧化氢的结构式,过氧化氢是共价化合物,其结构式为H-O-O-H;Y2X2是过氧化钠,过氧化钠是离子化合物,电子式为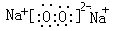 ;
;
(2)O与S的氢化物中,H2O的沸点较高,因为水分子间存在氢键;Z的低价氧化物是二氧化硫,转化为高价氧化物是三氧化硫,化学方程式为2SO2+O2 2SO3
2SO3
(3)Cl在元素周期表中的位置是第三周期第VIIA族;实验室用浓盐酸与二氧化锰加热制取氯气,化学方程式为4HCl(浓)+MnO2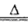 2H2O + Cl2↑+MnCl2;HCl中有1/2作还原剂,二氧化锰作氧化剂,所以该反应中氧化剂与还原剂的物质的量之比是1:2。
2H2O + Cl2↑+MnCl2;HCl中有1/2作还原剂,二氧化锰作氧化剂,所以该反应中氧化剂与还原剂的物质的量之比是1:2。
本题难度:一般
5、选择题 16O与18O是氧元素的两种核素,NA表示阿伏加德罗常数,下列说法正确的是
A.16O与18O互为同分异构体
B.16O与18O核外电子排布方式不同
C.通过化学变化可以实现16O与18O间的相互转化
D.标准状况下,1.12L16O2和1.12L18O2均含有0.1NA个氧原子
参考答案:D
本题解析:
正确答案:D
A、不正确,16O与18O是氧的两种核素,互为同位素;
B.不正确,16O与18O核外电子数相同,核外电子排布方式相同,均为1s22s22p4
C.不正确,通过化学变化无法实现16O与18O间的相互转化,只有通过核反应才能实现;
D.正确。
本题难度:一般