1、计算题 (8分)已知过氧化钠投入水中能发生下列反应:2Na2O2 + 2H2O =" 4NaOH" + O2↑。若7.8g过氧化钠投入足量水中,求生成NaOH 的物质的量和所生成的O2在标准状况下的体积。
参考答案:n(NaOH)=0.2mol? v(O2)= 1.12L
本题解析:设生成NaOH 的物质的量为x,所生成的O2在标准状况下的体积为y,则由
2Na2O2? +? 2H2O? =? 4NaOH? +? O2↑
2×78? 4? 22.4
7.8g?X? y
由比例关系式:
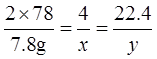 ?所以x= 0.2? y=1.12
?所以x= 0.2? y=1.12
点评:本题重点考查的是物质的量在化学计算中的应用,解答此类为题需要对定量关系一定要准确识记,会应用。
本题难度:一般
2、计算题 (6分)某液体化合物X2Y4,常用做火箭燃料。16 g X2Y4在一定量的O2中恰好完全燃烧,反应方程式为X2Y4(l)+O2(g)===X2(g)+2Y2O(l)。Y2O常温下为常见的液体。冷却后标准状况
下测得气体生成物的体积为11.2 L,则:
(1)求反应前O2在标准状况下的体积V(O2)。
(2)求X2的摩尔质量;X、Y分别为什么元素?(均要有推断过程。)
参考答案:(1)11.2 L;(2)28 g/mol;X为氢,Y为氮
本题解析:(1)由方程式可知,反应前后气体的体积不发生变化,X2和氧气的关系式为1:1,故V(O2)=V(X2)=11.2L,故答案为:11.2L;(2)标准状况下,气体摩尔质量M=Vm×ρ,气体X2的摩尔质量=22.4L/mol×1.25g/L=28g/mol,11.2L X2的物质的量=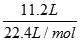 =0.5mol,n(X2Y4)=n(X2)=0.5mol,故Mr(X2Y4)=
=0.5mol,n(X2Y4)=n(X2)=0.5mol,故Mr(X2Y4)=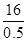 =32,则Y的相对原子质量=
=32,则Y的相对原子质量=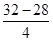 =1,故Y为氢元素,故答案为:28g/mol;氢.
=1,故Y为氢元素,故答案为:28g/mol;氢.
考点:化学方程式的有关计算
本题难度:一般
3、选择题 下列说法正确的是(? )
A.1molO的质量是16g/mol
B.Na+ 的摩尔质量是23g/mol
C.CO2的摩尔质量是44
D.氢的摩尔质量是2g/mol
参考答案:B
本题解析:A.1molO的质量是16g或O的摩尔质量是16g/mol。错误。B.Na+的摩尔质量是23g/mol正确。C.CO2的摩尔质量是44g/mol。错误。D.氢的摩尔质量是2?g/mol?概念不明确。是指的氢原子还是氢分子。错误。
本题难度:简单
4、选择题 将一定量的Na、Na2O、Na2O2的混合物与足量的水反应,在标准状况下得到a L混合气体。将该混合气体通过电火花引燃,恰好完全反应,则原混合物中Na、Na2O、Na2O2的物质的量之比可能为
A.2:1:3
B.1:1:2
C.1:2:1
D.2:3:1