1、填空题 (6分)在有机化学工业中常用的一种钠盐是NaBH4,即硼氢化钠。它具有很强的还原性,也是一种高贮氢密度材料,是最有可能作为氢燃料电池的即时供应氢源。但它不能与水和酸共存。⑴将其投入水中可生成偏硼酸钠(NaBO2)和氢气,写出该反应的化学方程式?,反应中的还原剂是?,每摩NaBH4反应时电子转移数为?mol。
⑵NaBH4还用于将含Au3+的碱性废液中回收黄金,其离子方程式为:
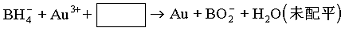
请写出配平的离子方程式?。
2、选择题 水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O +O2+xOH―
+O2+xOH―?Fe3O4+S4O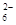 +2H2O,
+2H2O,
下列说法中,正确的是(?)?
A.每生成1mol Fe3O4,反应转移的电子总数为3mol ;
B.x="6"
C.1mol Fe2+被氧化时,被Fe2+还原的O2的物质的量为1/3mol;
D.Fe2+和S2O32―-都是还原剂;
3、选择题 下列实验现象与氧化还原反应有关的是
[ ? ]
A.碳酸钠中加入CaCl2溶液产生白色沉淀物
B.硫酸铜溶液中插入铁片,铁片上出现红色沉淀物
C.石灰石溶于盐酸并产生气泡
D.铁在氧气中燃烧,剧烈反应火星四射
4、选择题 把SO2通入Fe(NO3)3溶液中,溶液由棕色变为浅绿色,但立即又变为棕黄色,这时若滴入BaCl2溶液,会产生白色沉淀。在上述一系列变化过程中,最终被还原的是
[? ]
A.SO2
B.Cl-
C.Fe3+
D.NO3-
5、选择题 向含NaBr和NaI的溶液中,通入Cl2,充分反应后将所得的溶液蒸干、灼烧,将得到的固体冷却后称量。称量固体的质量与通入Cl2的体积关系如图所示:则原混合液中NaI的物质的量为
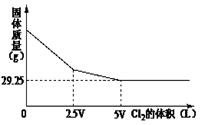
A.52.5g
B.60g
C.45g
D.37.5g