1、填空题 现有下列电解质溶液:① Na2CO3 ② NaHCO3 ③? ④CH3COONH4 ⑤NH4HCO3
④CH3COONH4 ⑤NH4HCO3
已知酸性H2CO3 >?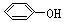 > HCO3-
> HCO3-
(1)常温下,物质的量浓度相同的① 、②、③溶液pH大小顺序为(填写序号):_____>_____>_____。
(2)写出⑤与足量NaOH溶液混合加热反应的离子方程式____________________。
(3)已知常温下CH3COONH4溶液呈中性,根据这一事实推测⑤溶液的pH_____7(填>、=或<)
(4)在温度t ℃时,pH=3的某水溶液中c(OH-)=10-9 mol/L在此温度下pH均为4的盐酸和(NH4)2SO4溶液中由水电离出的c(H+)之比为_________。
(5)将标准状况下的4.48 L氨气完全溶解在含0.1 mol HCl的水溶液中形成1 L溶液,所得溶液pH=9,其中离子浓度由大到小的顺序是_______________。
(6)常温下,pH=10的强碱AOH和pH=4的酸HnB等体积混合后溶液显酸性, AOH与HnB完全中和所得溶液呈_________性,其原因用离子方程式表示为__________________________。
参考答案:(1)①>③>②
(2)NH4++HCO3-+2OH- NH3↑+CO32-+2H2O
NH3↑+CO32-+2H2O
(3)>
(4)1:104
(5)c(NH4+)>c(Cl-)>c(OH-)>c(H+)?
(6)碱;Bn-+H2O HBn-1+OH-
HBn-1+OH-
本题解析:
本题难度:一般
2、简答题 (1)有下列物质①Cu②液态SO2③CH3COOH④NaHCO3⑤H2O⑥熔融NaCl⑦BaSO4属于弱电解质的是______(填序号)
(2)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:______.NaHCO3水解的离子方程式.
(3)常温下,将某一元酸HA和NaOH溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如表:
| 实验编号 | HA物质的量浓度(mol?L-1) | NaOH物质的量浓度(mol?L-1) | 混合溶液
的pH
a
0.1
0.1
pH=9
b
c
0.2
pH=7
|
请回答:
①从a组情况分析,HA是强酸还是弱酸______.
②b组情况表明,c______0.2(选填“大于”、“小于”或“等于”)混合溶液中离子浓度
c(A-)______c(Na+).(选填“大于”、“小于”或“等于”)
③a组实验所得混合溶液中由水电离出的c(OH-)=______mol?L-1.
参考答案:(1)弱电解质在水溶液中部分电离,存在电离平衡,满足该条件为:③CH3COOH、⑤H2O,故答案为:③⑤;
(2)常温下,0.1mol?L-1NaHCO3溶液的pH大于8,说明了HCO3-的水解程度大于其电离程度,则溶液中Na+、HCO3-、CO32-、OH-四种微粒的浓度由大到小的顺序为:c(Na+)>c(HCO3-)>c(OH-)>c(CO32-);碳酸氢钠溶液中HCO3-部分水解生成碳酸和氢氧根离子,其水解方程式为:HCO3-+H2O=H2CO3+OH-,
故答案为:c(Na+)>c(HCO3-)>c(OH-)>c(CO32-);HCO3-+H2O=H2CO3+OH-;
(3)①根据a可知:等体积等浓度混合,恰好生成正盐,溶液的pH=9,说明生成强碱弱酸盐,所以HA为弱酸,故答案为:HA是弱酸;
②若该酸为强酸,等体积等浓度混合时pH=7,而HA为弱酸,等体积等浓度混合溶液的pH大于7,则为保证pH=7,应使酸浓度应该大于0.2mol/L;
溶液的pH=7,溶液中c(H+)=c(OH-),由电荷守恒c(Na+)+c(H+)=c(A-)+c(OH-)可知:c(A-)=c(Na+),
故答案为:大于;等于;
③由a组实验所得混合溶液为NaA溶液,溶液pH=9,说明NaA为强碱弱酸盐,溶液中的氢氧根离子是水电离的,所以水电离的溶液中的c(OH-)=10-5mol/L,
故答案为:10-5.
本题解析:
本题难度:简单
3、选择题 温度相同、浓度均为0.2mol/L的①硫酸铵,②硝酸钠,③硫酸氢铵,④硝酸铵,⑤碳酸钠,⑥醋酸钠溶液,它们的pH由小到大的排列顺序是( )
A.①③⑥④②⑤
B.③①④②⑥⑤
C.③②①⑥②⑤
D.⑤⑥②④①③
参考答案:①(NH4)2SO4、④NH4NO3水解呈酸性,pH<7;③NH4HSO4电离出H+呈酸性,pH<7;
②NaNO3不水解,pH=7;
⑤Na2CO3,⑥CH3COONa,水解呈碱性,pH>7,
①、④比较,前者c(NH4+)大,水解生成c(H+)大,pH小,
①③比较,后者电离出c(H+)比前者水解出c(H+)大,pH小,
⑤⑥比较碳酸钠水解程度大于醋酸钠,溶液中氢氧根离子浓度⑤>⑥,
所以得到溶液PH有小到大的顺序为③①④②⑤⑥,
故选B.
本题解析:
本题难度:一般
4、选择题 30℃时,在0.1mol?L-1的Na2S、NaHS两溶液中均存在的关系是( )
A.c(H+)?c(OH-)=1×10-14
B.c(Na+)=c(S2-)+c(HS-)+c(H2S)
C.c(OH-)=c(H+)+c(HS-)+2c(H2S)
D.c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-)
参考答案:A.常温时,c(H+)?c(OH-)=1×10-14,温度升高促进水的电离,则30℃时,c(H+)?c(OH-)>1×10-14,故A错误;
B.根据物料守恒:在0.1mol?L-1的Na2S溶液中存在:c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),在0.1mol?L-1的NaHS溶液中存在:c(Na+)=c(S2-)+c(HS-)+c(H2S),故B错误;
C.根据质子守恒:在0.1mol?L-1的Na2S溶液中存在:c(OH-)=c(H+)+c(HS-)+2c(H2S),在0.1mol?L-1的NaHS溶液中存在:c(OH-)=c(H+)+c(H2S),故C错误;
D.从溶液呈电中性的角度分析,两溶液中均存在:c(Na+)+c(H+)=c(OH-)+c(HS-)+2c(S2-),故D正确.
故选D.
本题解析:
本题难度:简单
5、选择题 常温下将稀NaOH溶液和稀CH3COOH溶液混合,不可能出现的结果是( )
A.pH>7,且c(Na+)>c(OH-)>c(H+)>c(CH3COO-)
B.pH>7,且c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
C.PH<7,且c(CH3COO-)>c(H+)>c(Na+)>c(OH-)
D.pH=7,且c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
参考答案:A
本题解析:
本题难度:简单