1、选择题 下列各组溶液,只要用试管和胶头滴管,不用任何化学试剂就可以鉴别的是
A.KOH和Al2(SO4)3
B.稀H2SO4和NaHCO3
C.CaCl2和Na2CO3
D.Ba(OH)2和NaHSO4
参考答案:A
本题解析:KOH溶液滴到Al2(SO4)3溶液中先沉淀后溶解,Al2(SO4)3溶液滴到KOH溶液中,先无现象,后产生沉淀,A可以鉴别,其余无论谁滴谁现象都相同,无法鉴别。答案选A。
点评:不用任何试剂互相滴加可以鉴别的物质必须反应的现象不相同。
本题难度:一般
2、选择题 下列除杂的实验方法不正确的是?(?)?
A.除去镁粉中混有的少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥
B.除去Na2CO3固体中的NaHCO3:置于坩埚中加热
C.除去Fe3+中的Al3+:加入过量的氨水充分反应,过滤
D.除去FeCl3酸性溶液中的FeCl2:通入足量的Cl2
参考答案:C
本题解析:A正确,AL能与烧碱溶液反应而Mg不反应;B正确,利用NaHCO3固体不稳定受热易分解生成碳酸钠、二氧化碳和水;C错,Fe3+与Al3+均能与氨水反应生成沉淀;D正确,利用Fe2+的的还原性与强氧化性物质氯气发生氧化还原反应;
本题难度:简单
3、实验题 (8分)欲除去硝酸钾固体中混有的少量氯化钾杂质,某学生进行如下实验操作。回答下列问题:
⑴溶解样品。该过程所需的仪器有_______________________________________________。
⑵向溶解后的溶液中加入适量的 ____________ (填化学式)溶液,使氯化钾转化为沉淀。
⑶将混合液进行过滤,过滤装置和操作如图所示,指出图中的两处错误:
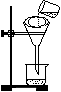
① _____________________________________?;
② _____________________________________?。
参考答案:(1)烧杯、玻璃棒(2分)
(2)AgNO3(2分)
(3)漏斗下端管口没有紧靠烧杯内壁;液体没有用玻璃棒引流(各2分)
本题解析:考查常见的基本实验操作。
(1)固体溶解应该在烧杯中,同时需要玻璃棒搅拌。
(2)由于不能引入新的杂质,所以应该加入适量的硝酸银溶液除去氯化钾。
(3)根据装置图可知,主要错误是漏斗下端管口没有紧靠烧杯内壁;液体没有用玻璃棒引流。
本题难度:一般
4、实验题 (10分)实验室现需配制物质的量浓度为1 mol・L-1的NaOH溶液480 mL。
(1)实验过程中用到的玻璃仪器有:烧杯、量筒、胶头滴管、________、________。
(2)要配制此溶液,需要称量NaOH固体的质量为________。
(3)配制好的NaOH溶液不能用带磨口玻璃塞的试剂瓶存放,请解释原因(用化学方程式表示)________________________________。
(4)若将此溶液长期暴露在空气中,最终转化为________,取一定量的该物质溶于水配制成饱和溶液,通入CO2气体后发现溶液变浑浊,写出发生反应的化学方程式
____________________________________。
参考答案:(1)500 mL容量瓶 玻璃棒
(2)20 g
(3)SiO2+2NaOH===Na2SiO3+H2O
(4)Na2CO3 Na2CO3+CO2+H2O===2NaHCO3↓?
本题解析:实验室容量瓶的容量有50 mL、100 mL、150 mL、200 mL、250 mL、500 mL、1 000 mL等,另外需要注意,所配溶液体积大于所需溶液体积;NaOH溶液能腐蚀玻璃,可用玻璃瓶保存,但不能用磨口玻璃塞;NaOH溶液在空气中吸收CO2而变成Na2CO3,Na2CO3饱和溶液中通入CO2气体后,生成溶解度较小的NaHCO3晶体,而使溶液变浑浊。
本题难度:一般
5、选择题 下列物质含氢原子数最多的是
A.1 mol H2
B.0.5 mol NH3
C.6.02×1023个的CH4分子
D.0.3 mol H3PO4
参考答案:C
本题解析:试题分析:根据物质的化学式可知,1mol 氢气分子中含有2mol氢原子;0.5mol 氨气分子中1.5mol 氢原子;6.02×1023个的CH4分子物质的量是1mol,含有4mol 氢原子;0.3mol磷酸中含有0.9mol 氢原子,则物质含氢原子数最多的是氯化氢,答案选C。
考点:考查物质的量的有关计算
点评:该题是高考中的常见考点和基本题型,属于基础性试题的考查,难度不大。主要是考查学生对以物质的量为核心的有关计算的熟悉掌握程度,有利于培养学生的应试能力和学习效率。
本题难度:一般