1、实验题 (15分)某同学设计了以下操作流程来除去混在氯化钠固体中的少量硫酸钠和氯化钙。

(1)试剂A是?,试剂C是?。
(2)操作a的名称是?,操作a得到的滤渣的成分是?。
(3)加入试剂C调节滤液PH的目的是?。
(4)操作b中用到的主要仪器为酒精灯、?、三脚架和玻璃棒。
该同学想利用上述得到的氯化钠设计一套实验装置来电解饱和食盐水,并检验氯气的氧化性和测定所产生的氢气的体积(约8mL)。
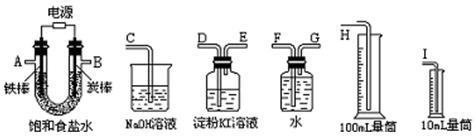
(5)试从上图中选用几种必要的仪器,连成一整套装置,各种仪器接口的连接顺序(填编号)是:A接__?_?,?接___?;B接___?,?接__?_?;
(6)铁棒接直流电源的________极;炭棒上发生的电极反应为?;
(7)能说明氯气具有氧化性的实验现象是_________________________?________?;
(8)若装入的饱和食盐水为75mL(电解前后溶液体积变化可忽略,假设两极产生的气体全部逸出),当测得氢气为8.4mL(标准状况)时停止通电。将U形管内的溶液倒入烧杯,其pH约为___。
参考答案:(1)BaCl2或Ba(OH)2, HCl(2)过 滤? CaCO3、BaCO3 和BaSO4
滤? CaCO3、BaCO3 和BaSO4
(3)除去过量的Na2CO3,提纯NaCl?(4)蒸发皿
(5)G、F、I? D、E、C
(6)负极? 2Cl-―2e →Cl2↑
(7)KI淀粉溶液变蓝
(8)12
本题解析:略
本题难度:一般
2、填空题 回答下面问题:
(1)分离沸点不同但又互溶的液体混合物,常用什么方法?______________________
(2)在分液漏斗中用一种有机溶济提取水溶液里的某物质时,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法。________________________________
参考答案:(1)蒸馏方法
(2)取一支小试管,打开分液漏斗的活塞,慢慢放出少量液体,往其中加入少量水,如果加水后,试管中的液体不分层,说明分液漏斗中,下层是“水层”,反之,则上层是水层。
本题解析:
本题难度:一般
3、选择题 对于某些离子的检验及结论一定正确的是
A.加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42-
B.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
C.加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32-
D.加入碳酸钠溶液产生白色沉淀,再加盐酸,白色沉淀消失,一定有Ba2+
参考答案:B
本题解析:A、氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀,故A错误;B、湿润红色石蕊试纸遇碱性物质变蓝,即产生的气体是氨气,因此一定含有铵根离子,故B正确;C、盐酸能与含碳酸根或碳酸氢根离子的物质反应生成二氧化碳,故C不正确;D、碳酸钠能与含可溶性钙离子或钡离子的物质结合生成沉淀,故D错误,答案选B。
本题难度:一般
4、选择题 下列有关实验原理、方法和结论都正确的是
A.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+
B.取少量X溶液,加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中一定含有Fe2+
C.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则说明原溶液中一定含SO42-
D.某无色溶液用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液含有Na+无K+
参考答案:A
本题解析:A.加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,这说明气体一定是氨气,所以一定有NH4+,A正确;
B.取少量X溶液,加入适量新制氯水,再加几滴KSCN溶液,溶液变红,说明X溶液中可能含有Fe2+,也可能含有铁离子,B不正确;
C.向某溶液中滴加BaCl2溶液,若有白色沉淀,再滴加足量稀HNO3,若沉淀不溶解,则原溶液中可能含SO42-,也可能含有Ag+,C不正确;
D.某无色溶液用洁净铂丝蘸取溶液进行焰色反应,火焰呈黄色,则原溶液含有Na+,但不能确定是否含有K+,乙烷没有透过蓝色的钴玻璃观察,D不正确,答案选A。
点评:该题是中等难度的试题,试题综合性强,对学生的思维能力要求高,有利于培养学生的逻辑推理能力和规范严谨的实验设计能力。该类试题需要明确的是进行物质的检验时,要依据物质的特殊性质和特征反应,选择适当的试剂和方法,准确观察反应中的明显现象,如颜色的变化、沉淀的生成和溶解、气体的产生和气味、火焰的颜色等,进行判断、推理、验证即可。
本题难度:一般
5、选择题 除去下列物质中含有的少量杂质(括号中的物质) 的方法中错误的是?
[? ]
A.H2( HCl)通过水洗涤
B.NO(NH3)通过水洗涤
C.NH4Cl( NaCl)加热混合物
D.NH4Cl溶液(I2)用CCl4萃取
参考答案:C
本题解析:
本题难度:一般