|
|
|
高中化学知识点总结《燃烧热》考点特训(2020年冲刺版)(五)
2020-08-23 07:18:45
【 大 中 小】
|
1、选择题 已知Ba(AlO2)2可溶于水。下图表示的是向含A12(SO4)3 0.01mol的溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系(其中a、c分别是0b段和bd段的中点)。下列有关叙述正确的是
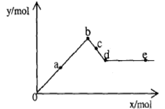
A.a时沉淀的质量为3.495 g
B.b时沉淀的物质的量为0.05 mol
C.c时溶液中Ba2+离子的物质的量为0.005 mol
D.e时溶液中AlO2―的物质的量为0.01 mol
2、选择题 下列关于能源和作为能源物质的叙述中不正确的是( )
A.化学反应中的能量变化通常表现为热量的变化
B.天然气、石油、流水、风力为一次能源。
C.需要加热才能发生的反应一定是吸热反应
D.反应物总能量和生成物总能量的相对大小决定了反应是放出能量还是吸收能量
|
3、选择题 在同温同压下,下列各组热化学方程式中 Q1 <Q2的是(反应条件已略去)
A.2H2(g) + O2(g) = 2H2O(g) ;△H=-Q1 , 2H2(g) + O2(g) = 2H2O(l) ;△H=-Q2
B.S(g) + O2(g) = SO2(g) ;△H=-Q1 , S(s) + O2(g) = SO2(g) ;△H=-Q2
C.C(s) + 1/2O2(g) =" CO(g)" ;△H=-Q1 , C(s) + O2(g) = CO2(g) ;△H=-Q2
D.H2(g) + Cl2(g) =" 2HCl(g)" ;△H=-Q1 , 1/2H2(g) + 1/2Cl2(g) =" HCl(g)" ;△H=-Q2
|
4、填空题 中学化学实验中,淡黄色的pH试纸常用于测定溶液的酸碱性。在25 ℃时,若溶液的pH=7,试纸不变色;若pH<7,试纸变红色;若pH>7,试纸变蓝色。而要精确测定溶液的pH,需用pH计。pH计主要通过测定溶液中H+浓度来测定溶液的pH。
(1)已知水中存在平衡:H2O H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。
A.向水中加入NaHSO4
B.向水中加入Cu(NO3)2
C.加热水至100 ℃[其中c(H+)=1×10-6 mol・L-1]
D.在水中加入(NH4)2SO4
(2)现欲测定100 ℃沸水的pH及酸碱性,若用pH试纸测定,则试纸显?色,溶液呈?性(填“酸”、“碱”或“中”);若用pH计测定,则pH?7(填“>”、“<”或“=”),溶液呈?性(填“酸”、“碱”或“中”)。
5、选择题 常温下,某溶液中由水电离出来的c(OH-)=1×10―11 mol/L,若向该溶液中滴入2―3滴酚酞,溶液的颜色可能是?(?)
mol/L,若向该溶液中滴入2―3滴酚酞,溶液的颜色可能是?(?)
A.只显红色
B.呈无色
C.无色或粉红
D.红色或无色
 H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。
H++OH- ΔH>0,现欲使平衡向右移动,且所得溶液呈酸性,选择的方法是?(填字母)。 mol/L,若向该溶液中滴入2―3滴酚酞,溶液的颜色可能是?(?)
mol/L,若向该溶液中滴入2―3滴酚酞,溶液的颜色可能是?(?)