|
|
|
高考化学知识点归纳《化学反应与能量》在线测试(2020年最新版)(四)
2020-08-23 07:25:05
【 大 中 小】
|
1、选择题 炼金厂的废水中含有CN-有剧毒,其性质与卤素离子相似,还原性介于I-与Br-之间,HCN为弱酸.下列说法不正确的是
A.CN-可以和稀硫酸反应生成HCN
B.CN-可被Cl2氧化成(CN)2
C.在水溶液中(CN)2可被F-还原
D.常温下NaCN溶液显碱性
参考答案:C
本题解析:分析:A、HCN为弱酸,利用强酸制取弱酸的原理来分析;
B、CN-的还原性介于I-与Br-之间,利用氧化还原反应来分析;
C、利用氧化性的强弱来分析氧化还原反应;
D.氰化钠是强碱弱酸盐,根据盐的类型判断.
解答:A、HCN为弱酸,根据强酸制弱酸规律可知,CN-可以和稀硫酸反应生成HCN,故A正确;
B、由于CN-的还原性介于I-与Br-之间,则Cl2可氧化CN-而生成(CN)2,故B正确;
C、因F-的还原性弱于CN-,故(CN)2与F-不反应,故C错误;
D.氰化钠是强碱弱酸盐,CN-易水解而使其溶液呈碱性,故D正确;
故选C.
点评:本题考查学生利用信息中离子的性质的相似性及氧化还原反应来分析解答问题,明确信息的应用,并熟悉强酸制取弱酸、氧化性、还原性的强弱等知识来解答.
本题难度:简单
2、选择题 已知CH4(g)+2O2(g)=2CO2(g)+2H2O(l);△H=-Q1kJ/mol,2H2(g)+O2(g)=2H2O(g) ;△H=-Q2 kJ/mol,2H2(g)+O2(g)=2H2O(l) ;△H=-Q3 kJ/mol,常温下取体积比为4:1的CH4和H2的混合气11.2L(标况)经完全燃烧后恢复至常温,放出的热量是?( ?)?
A.0.4Q1+0.05Q3
B.0.4Q1+0.05Q2
C.0.4Q1+0.1Q3
D.0.4Q1+0.2Q2
参考答案:A
本题解析:试题分析:混合气的物质的量是0.5mol,其中甲烷是0.4mol,氢气是0.1mol。由于是恢复到常温下,所以生成物水是液态,因此反应中放出的热量是0.4Q1+0.05Q3,答案选A。
考点:考查反应热的有关计算
点评:该题是常识性知识的考查,试题基础性强,难度不大。该题的关键是明确水的状态,然后根据题意列式计算即可。
本题难度:困难
3、选择题 在烃分子中去掉2个氢原子形成一个双键是吸热反应,大约需要117 kJ ・mol-1~125 kJ ・mol-1 的热量,但1,3-环己二烯失去2个氢原子形成苯是放热反应,反应热是23.4 kJ ・mol-1 ,这表明
A.苯比1,3-环己二烯稳定
B.苯加氢生成环己烷是吸热反应
C.1,3-环己二烯比环己烷稳定
D.1,3-环己二烯加氢是吸热反应
|
参考答案:A
本题解析:A、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故A正确;
D、根据题意信息:烃分子中去掉两个氢原子形成一个双键是吸热反应,所以1,3-环已二烯加上两个氢原子是放热反应,故D错误;
B、根据题意信息可知,烃分子中去掉两个氢原子形成一个双键是吸热反应,所以烃分子中一个双键加上两个氢原子是放热反应,故B错误;
C、1,3-环已二烯失去两个氢原子变成苯是放热反应,说明1,3-环已二烯的能量高于苯的,能量越低越稳定,所以苯更稳定,故C错误。
故选A。
考点:吸热反应和放热反应 化学能与热能的相互转化
点评:本题考查学生吸热反应和放热反应的有关知识,可以根据所学知识来回答,难度不大。
本题难度:简单
4、填空题 已知:
2H2(气)+O2(气)=2H2O(气)+Q1?2H2(气)+O2(气)=2H2O(液)+Q2
2CO(气)+O2(气)=2CO2(气)+Q3
(1)关于Q1和Q2的关系正确的是______。
A.Q1>Q2
B.Q1<Q2
C.Q1=Q2
D.无法比较
|
你选择该答案的理由是______。
(2)CO和H2分别燃烧生成CO2和H2O(气),欲得到相同的热量,所需CO和H2的体积比是______。
参考答案:(1)B.液态水变成气态水需吸收热量或气态水变成液态水能放出热量;(2)Q1∶Q3。
本题解析:(1)由于状态不同,反应热不同,所以写热化学方程式时,一定要注明各物质的聚集状态。否则判为错误(注:偶有通常状况为气体的物质不写其状态,即默认为气体);(2)设CO为nCOmol,H2为nH2mol,因气体的体积比等于物质的量之比(T,P一定时)。由题可知:
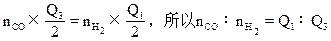
本题难度:一般
5、填空题 (8分)有效地利用现有新能源和开发新能源已受到各国的重视。
(1)工业上可用改进汽油组成的办法来改善汽油的燃烧性能。例如,加入CH30C(CH3)3,来生产无铅汽油”。 H3COC(CH3)3分子必存在的原子间连接形式有 。(填写编号,多选不得分)
①>C=0 ②>C=C< ③ ④
④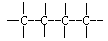
(2)天然气的燃烧产物无毒、热值高、管道输送方便,将成为我国西部开发的重点之一,天然气常和石油伴生,其主要的成分是甲烷。能说明它是正四面体而非正方形平面结构的理由是 。(填写编号)
①其一氯取代物不存在同分异构体 ②其二氯取代物不存在同分异构体
(3)1980年我国首次制成一辆燃氢汽车,乘员12人,以50km/h行驶了40km。为了有效发展民用氢能源,首先必须制得廉价的氢气。下列可供开发又较经济的制氢方法是
①电解水 ②锌和稀硫酸反应 ③光解海水
(4)其次,制得纯氢气后,还需要解决的问题是 。(写出其中的一个)
参考答案:(1)③ (2) ② (3)③(4)氢气的储存和运输
本题解析:(1)根据H3COC(CH3)3分子的结构简式可判断,分子全部是单键形成的,①②不正确。分子中不含羟基,所以④不正确。答案选③。
(2)如果甲烷是正方形平面结构,则其二氯取代物就存在两种同分异构体。所以答案选②。
(3)电解水需要消耗大量的电脑,不正确。锌和稀硫酸反应,生成的气体少,不能满足需要。所以正确的答案是③。
(4)得到氢气后人类还需解决的问题是氢气的储存和运输问题。因为氢气是很活泼的气体,容易燃烧和爆炸,不易大量储存和运输。
本题难度:一般
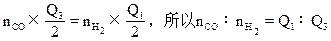
 ④
④