1��ѡ���� ���������к��й��ۼ������ӻ������ǣ���?��
��MgF2?��Na2O2��NaOH?��NH4Cl?��CO2?��H2O2?��N2
A���ڢۢܢݢ�
B���٢ڢۢܢ�
C���ڢۢ�
D���٢ۢݢ�
�ο��𰸣�C
���������һ����õĽ����ͻ��õķǽ��������γ����Ӽ����ǽ���Ԫ�ص�ԭ�Ӽ������γɹ��ۼ�������Ϊ�������Ӽ��Ļ����������ӻ����ȫ���ɹ��ۼ��γɵĻ������ǹ��ۻ�������Ժ��й��ۼ������ӻ������Ǣڢۢܡ�����ֻ�����Ӽ����ݢޢ���ֻ�й��ۼ�����ѡC��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣�����ۺ���ǿ�����ض�ѧ�������������ͽ��ⷽ����ָ����ѵ��������Ĺؼ�����ȷ��ѧ���뻯����Ĺ�ϵ��Ȼ��������ü��ɣ�����������ѧ������˼ά���������Ӧ��������
�����Ѷȣ���
2��ѡ���� ij�»���ͻ�����ʵĽṹ��ʽ��ͼ��������ط�����ȷ����
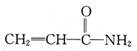
A���縺�ԣ�C<N<O
B���÷����ЦҼ���м���Ŀ֮��Ϊ4:2
C���÷�������ԭ�Ӵ���ͬһƽ��
D���÷��ӵļӾ۲���Ϊ
�ο��𰸣�A
���������A��ͬ��������Ԫ�أ�����ԭ�����������縺���������Ե縺�ԣ�C<N<O����ȷ��B�����ݽṹ��ʽ��֪���÷����ЦҼ�9�����м�2����������Ŀ֮��Ϊ9:2������C��Nԭ������Χ��ԭ�Ӳ���ͬһƽ���ϣ�����D���Ӿۺ�����Ϊ��CH2��CH��������
�����Ѷȣ�һ��
3��ѡ���� �����йئҼ��ͦм���˵����ȷ����
A���Ҽ��Ǿ���Գƣ����м�����Գ�
B���м���������p���ӡ�ͷ��ͷ���ص��γɵ�
C���Ҽ����ؼ���������ת����Ӱ�����ǿ��
D���м��ȦҼ��ص��̶ȴ��γɵĹ��ۼ�ǿ
�ο��𰸣�C
����������Ҽ��ǡ�ͷ��ͷ���ص��γɣ����ؼ���������ת��Ϊ��Գƣ����м���������p���ӡ��粢�硱�ص��γɣ��ص��̶�С��Ϊ����Գƣ��ݴ������A���Ҽ�����Գƣ����м��Ǿ���Գƣ���A����B���м���������p���ӡ��粢�硱�ص��γɣ���B����C���Ҽ�Ϊ��Գƣ����ؼ���������ת����Ӱ�����ǿ�ȣ���C��ȷ��D���м��ȦҼ��ص��̶�С���γɵĹ��ۼ����ȶ�����D����ѡC��
�����Ѷȣ�һ��
4��ѡ���� ���з�Ӧ�У��������뻹ԭ�����ʵ����Ĺ�ϵΪ1��2����
A.N2O+4H2�T2NH3+H2O
B.2CH3COOH+Ca��ClO��2�T2HClO+Ca��CH3COO��2
C.I2+2NaClO3�T2NaIO3+Cl2
D.4HCl+MnO2�TMnCl2+Cl2��+2H2O
�ο��𰸣�D
�������������������Ԫ�ػ��ϼ۽��͵ķ�Ӧ����������������Ԫ�ػ��ϼ����ߵķ�Ӧ���ǻ�ԭ����
A����Ӧ�е�Ԫ�ػ��ϼ���N2O��+1�۽���ΪNH3��-3�ۣ�N2O������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ԫ�ػ��ϼ���H2��0������ΪNH3��H2O��+1�ۣ�H2�ǻ�ԭ������Ԫ�ػ��ϼ�ȫ�����ߣ����ݻ�ѧ�������жϣ�
B�����ڸ��ֽⷴӦ������������ԭ��Ӧ��
C����Ӧ����Ԫ�ػ��ϼ���NaClO3��+5�۽���ΪCl2��0�ۣ�NaClO3������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ӧ�е�Ԫ�ػ��ϼ���I2��0������ΪNaIO3��+5�ۣ�I2�ǻ�ԭ������Ԫ�ػ��ϼ�ȫ�����ߣ���ϻ�ѧ�������жϣ�
D����Ӧ4HCl+MnO2�TMnCl2+Cl2��+2H2O�У���Ԫ�ػ��ϼ���MnO2��+4�۽���ΪMnCl2��+2�ۣ�MnO2������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ӧ����Ԫ�ػ��ϼ���HCl��-1������ΪCl2��0�ۣ�HCl�ǻ�ԭ�����ɷ���ʽ��������Ԫ�ػ��ϼۿ�֪�� ��HCl��ԭ�����ã���
��HCl��ԭ�����ã��� ��HCl�������ã���ϻ�ѧ�������жϣ�
��HCl�������ã���ϻ�ѧ�������жϣ�
���A����ӦN2O+4H2�T2NH3+H2O�У���Ԫ�ػ��ϼ���N2O��+1�۽���ΪNH3��-3�ۣ�N2O������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ԫ�ػ��ϼ���H2��0������ΪNH3��H2O��+1�ۣ�H2�ǻ�ԭ������Ԫ�ػ��ϼ�ȫ�����ߣ������������뻹ԭ�������ʵ���֮��Ϊ1��4����A����
B�����ڸ��ֽⷴӦ������������ԭ��Ӧ����̸�������뻹ԭ������B����
C����ӦI2+2NaClO3�T2NaIO3+Cl2�У���Ԫ�ػ��ϼ���NaClO3��+5�۽���ΪCl2��0�ۣ�NaClO3������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ӧ�е�Ԫ�ػ��ϼ���I2��0������ΪNaIO3��+5�ۣ�I2�ǻ�ԭ������Ԫ�ػ��ϼ�ȫ�����ߣ������������뻹ԭ�������ʵ���֮��Ϊ2��1����C����
D����Ӧ4HCl+MnO2�TMnCl2+Cl2��+2H2O�У���Ԫ�ػ��ϼ���MnO2��+4�۽���ΪMnCl2��+2�ۣ�MnO2������������Ԫ�ػ��ϼ�ȫ�����ͣ���Ӧ����Ԫ�ػ��ϼ���HCl��-1������ΪCl2��0�ۣ�HCl�ǻ�ԭ�����ɷ���ʽ��������Ԫ�ػ��ϼۿ�֪�� ��HCl��ԭ�����ã���
��HCl��ԭ�����ã��� ��HCl�������ã������������뻹ԭ�������ʵ���֮��Ϊ1��4��
��HCl�������ã������������뻹ԭ�������ʵ���֮��Ϊ1��4�� =1��2����D��ȷ��
=1��2����D��ȷ��
��ѡ��D��
����������������ԭ��Ӧ������������㣬�ѶȲ�������ݻ�ѧ�������ж��������뻹ԭ����ϵ��Ҳ���Ը��ݵ���ת���غ���㣬ע��D���Ȼ�������ã�
�����Ѷȣ�����
5������� (8��)��50mL0.50mol/L������50mL0.55mol/LNaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��
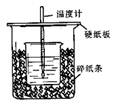
ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȡ��ش��������⣺
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
��2���ձ���������ֽ���������� ��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ (�ƫ��ƫС����Ӱ�족)
��4�������60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������� (���ȡ�����ȡ�)�������к��� (���ȡ�����ȡ�)����������
��5������ͬŨ�Ⱥ�����İ�ˮ(NH3��H2O)����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ�� �����ƫ����ƫС��������Ӱ�족����
�ο��𰸣�17.(8��)��1�����β�������� ��2������ʵ������е�������ʧ�� ��3��ƫС
��4������ȣ���ȣ���Ϊ�к�����ָ�������кͷ�Ӧ����1molH2O���ų���������������������
��5��ƫС��
�����������1���������ȼƵĹ����֪��װ�õ�ȱ�������ǻ��β�������������Ϊ�����β�������������2���к��Ȳⶨʵ��ɰܵĹؼ��DZ��¹�������С�ձ�֮��������ֽ���������ǣ�����ʵ������е�������ʧ����Ϊ������ʵ������е�������ʧ����3�����ձ����粻��Ӳֽ�壬�ᵼ������ɢʧ����õ��к�����ֵƫС����4����Ӧ�ų����������������Լ�������Ķ����йأ�����60mL0.50mol/L������50mL0.55mol/LNaOH��Һ���з�Ӧ��������ʵ����ȣ�����ˮ�������࣬���ų�������ƫ�ߣ������к��ȵľ���ǿ���ǿ�Ӧ����1molˮʱ�ų����ȣ������������أ�������60mL0.50mol/L������50mL0.55mol/LNaOH��Һ��Ӧ������к�����ֵ��ȣ���Ϊ������ȣ���ȣ���Ϊ�к�����ָ�������кͷ�Ӧ����1molH2O���ų��������������������أ���5����ˮΪ����������Ϊ���ȹ��̣�����ˮ����NaOH��Һ��Ӧ����Ӧ�ų�������С��57.3kJ����Ϊ��ƫС.
���㣺�����к��ȵIJⶨ��
�����Ѷȣ�һ��