1、简答题 短周期元素X、Y、Z组成的化合物Y2X和ZX2.Y2X溶于水形成的溶液能与ZX2反应生成一种化合物Y2ZX3.已知三种元素原子的质子总数为25,且Z和Y的原子序数之和比X的原子序数2倍还多1,Z原子有2个电子层,最外层电子数是核外电子数的
倍,试回答:
(1)X、Y、Z元素的名称:X______Y______Z______
(2)用电子式表示ZX2的形成过程:______
(3)Y2X对应水化物的电子式______,其中存在的化学键有______.
(4)写出Y2X溶于水的溶液与ZX2反应的化学方程式______.
参考答案:Z原子有2个电子层,最外层电子数是核外电子数的23倍,令最外层电子数为a,则23(2+a)=a,解得a=4,所以Z为C元素;
设X原子的质子数为x,Y原子的质子数为y.
三种元素原子的质子总数为25,则有6+x+y=25;
Z和Y的原子序数之和比X的原子序数2倍还多1,则有6+y=2x+1
联立方程解得:x=8,y=11,即X为氧元素,Y为钠元素.
(1)由上述分析可知,X为氧元素,Y为钠元素,Z为碳元素.
故答案为:氧;钠;碳.
(2)ZX2是CO2,CO2是共价化合物,碳原子与氧原子之间形成2对共用电子对,CO2形成过程为
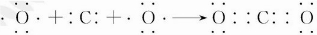
故答案为:
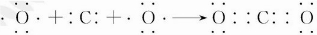
.
(3)Y2X为Na2O,对应水化物为NaOH,NaOH是离子化合物,由钠离子与氢氧根离子构成,氢氧化钠电子式为

. 钠离子与氢氧根离子之间为离子键,氢氧根离子中氢原子与氧原子之间为共价键.
故答案为:

;离子键、共价键.
(4)Y2X为Na2O,溶于水得NaOH溶液,ZX2是CO2,CO2与NaOH溶液反应生成碳酸钠与水,
反应方程式为2NaOH+CO2=Na2CO3+H2O.
故答案为:2NaOH+CO2=Na2CO3+H2O.
本题解析:
本题难度:一般
2、简答题 已知由短周期元素组成的A、B、C、D四种化合物所含原子数目依次为2、3、4、5,其中A、B、C含有18个电子,D含有10个电子.请回答
(1)A、B、D的化学式分别是A______;B______;D______.?
(2)已知8gD与O2完全反应,生成稳定化合物时放出445kJ的热量,写出反应的热化学方程式______.
(3)若C为第一和第二周期元素组成的化合物.
①C的溶液中加入少量的二氧化锰,有无色气体生成,写出化学方程式______;
②C的溶液中加入足量二氧化锰和稀硫酸,二氧化锰逐渐溶解生成Mn2+,反应中二氧化锰做______剂;
③当C分别发生①和②两个反应时,若都有1molC完全反应,①和②两个反应中转移电子数之比是:______.
参考答案:(1)由短周期两原子组成的18电子的化合物为HCl,三原子组成的18电子的化合物为H2S,四原子组成的18电子化合物为PH3或H2O2,由短周期五原子组成的10电子的化合物为CH4.A、B、D四种化合物所含原子数目依次为2、3、5,其中A、B含有18个电子,D含有10个电子,故A为HCl,B为H2S,D为CH4.
故答案为:HCl、H2S、CH4.
(2)8gCH4的物质的量为8g16g/mol=0.5mol,根据题意1molCH4完全燃烧放出热量为:1mol0.5mol×445kJ=-890kJ,则其反应的热化学方程式为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ?mol-1.
故答案为:CH4(g)+2O2(g)=CO2(g)+2H2O(l);△H=-890kJ?mol-1.
(3)若C为第一和第二周期元素组成的化合物,则C为H2O2.
①H2O2在二氧化锰作用下会迅速产生氧气:2H2O2?MnO2?.?2H2O+O2↑;
故答案为:2H2O2?MnO2?.?2H2O+O2↑.
②H2O2溶液中加入足量二氧化锰和稀硫酸,二氧化锰逐渐溶解生成Mn2+,锰元素化合价降低,二氧化锰做氧化剂;
故答案为:氧化剂.
③对于反应2H2O2?MnO2?.?2H2O+O2↑,1molH2O2完全反应,转移电子1mol,对于反应H2O2+MnO2+H2SO4=MnSO4+2H2O+O2↑,1molH2O2完全反应,转移电子2mol,两个反应中转移电子数之比是1:2.
故答案为:1:2.
本题解析:
本题难度:一般
3、选择题 下列说法正确的是( )
A.溶液中c(H+)>c(OH-),该溶液不一定显酸性
B.向沸腾的NaOH溶液中滴加FeCl3饱和溶液,可制备Fe(OH)3胶体
C.主族元素的简单离子R2-和M+的电子层结构相同,则原子序数R>M
D.若相同温度和浓度的两种酸的酸性HA>HB,则钠盐溶液的碱性NaA<NaB
参考答案:A.溶液的酸碱性取决于溶液中H+和OH-浓度的大小关系,溶液中c(H+)>c(OH-),溶液一定显酸性,故A错误;
B.制备Fe(OH)3胶体,应在沸水中滴加饱和的FeCl3溶液,当溶液呈红棕色时停止加热,如用NaOH溶液,易生成沉淀,故B错误;
C.主族元素的简单离子R2-和M+的电子层结构相同,则Z(R)+2=Z(M)-1,原子序数M>R,故C错误;
D.酸越弱,对应的盐溶液水解程度越大,则若相同温度和浓度的两种酸的酸性HA>HB,则钠盐溶液的碱性NaA<NaB,故D正确.
故选D.
本题解析:
本题难度:简单
4、选择题 XY2是由短周期元素形成的化合物,Y-比X2+多一个电子层,它与氩原子的电子层结构相同.下列有关叙述不正确的是( )
A.Y是第ⅦA族元素
B.X是第二周期元素
C.Y-与X2+的最外层电子数相同
D.化合物XY2的化学键为离子键
参考答案:XY2是由短周期元素形成的化合物,Y-比X2+多一个电子层,它与氩原子的电子层结构相同,则Y为Cl元素,Y-比X2+多一个电子层,X2+有两个电子层,X原子失去两个电子变为X2+,则X的Mg元素,
A.Y是Cl元素,其最外层有7个电子,为第VIIA族元素,故A正确;
B.X是Mg元素,位于第三周期,故B错误;
C.Y-与X2+的最外层电子数都是8,故C正确;
D.化合物氯化镁是由镁离子和氯离子构成的,氯离子和镁离子形成离子键,故D正确;
故选B.
本题解析:
本题难度:简单
5、选择题 下列说法中肯定错误的是
[? ]
A.某原子K层上只有1个电子
B.某原子M层上电子数为L层上电子数的4倍
C.某离子M层和L层的电子数均为K层的4倍
D.某离子的核电荷数与最外层电子数相等
参考答案:B
本题解析:
本题难度:一般