1、简答题 为了达到下表中的实验要求,请选择合适的化学试剂及实验方法,将其标号填入对应的空格中.
| 实验目的 |
试剂及方法
测定某废水的pH
检验早晨的自来水是否含Cl2分子
对蛋白质溶液进行分离提纯
检验胃舒平是否含有碳酸氢钠
|
A、将样品滴在淀粉碘化钾试纸上
B、将样品加入盐酸中
C、将样品 滴在广泛pH试纸上
D、在样品加入浓的硫酸铵溶液.
参考答案:用PH试纸测定废水的pH,然后与比色卡比较可判断废水的PH,故选C;
氯气具有强氧化性,用淀粉碘化钾试纸检验,生成单质碘,试纸变蓝,故选A;
蛋白质属于胶体,难溶于饱和硫酸铵溶液,可利用盐析的方法进行分离,故选D;
碳酸氢钠易与盐酸反应生成二氧化碳气体,溶液产生气泡,故选B.
故答案为:C;A;D;B.
本题解析:
本题难度:一般
2、选择题 下列实验的设计不可行的是
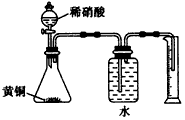
[? ]
A.向生石灰上滴加浓氨水可以制取少量的NH3
B.用水就能一次性鉴别溴苯、苯、乙酸三种物质
C.用如图所示的装置测定黄铜(Cu、Zn合金)中Zn的含量
D.为了除去Na2SO4溶液中的Na2SO3,应加入H2O2
参考答案:C
本题解析:
本题难度:一般
3、实验题 某学生为验证苯酚、醋酸、碳酸的酸性强弱,经过慎重考虑,设计如下实验装置:请回答下列问题
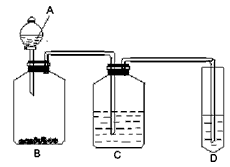
(1)各仪器中所盛放的药品是A______C______D______,(将序号填入横线上 ①苯酚 ②醋酸 ③碳酸
④Na2CO3 ⑤NaHCO3 ⑥苯酚钠)
(2) 装置C的作用____________。
(3) 试描述能证明三种酸的酸性强弱的现象____________。
(4)写出装置D中发生反应的化学方程式__________________。
参考答案:(1)②;⑤;⑥
(2)除去CO2中的氯化氢
(3)B装置中有气泡,D装置溶液变浑浊
(4)C6H5ONa?+CO2+H2O==C6H5OH+NaHCO3
本题解析:
本题难度:一般
4、实验题 某校研究性学习小组同学在实验时把一定量的SO2通入装有一定浓度BaCl2溶液的试管中,出现了白色浑浊物。
⑴实验小组的同学查阅了工具书上的相关数据,经过计算推导得出:即使把SO2通入BaCl2溶液中至饱和,也不可能生成BaSO3,故白色浑浊物只能是BaSO4。你认为所查阅的数据为:
SO2的溶解度、SO2饱和溶液中各离子的浓度以及_______________。
⑵小组同学对白色浑浊物成分及产生原因进行了各种合理的假设,并分别设计实验验证假设如下:
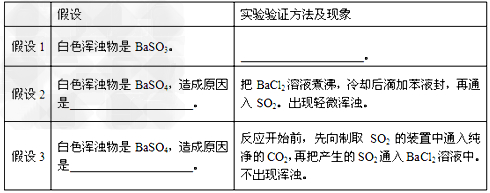
请把上表填充完全。
⑶写出在验证假设2的实验时,溶液中发生的反应的化学方程式:________________、
_______________;
⑷请你再提供一种假设。白色浑浊物是BaSO4,造成原因是________________。
参考答案:⑴BaSO3的溶度积或BaSO3的溶解度?
⑵假设1:在白色浑浊物中加入过量盐酸,变澄清;假设2:BaCl2溶液中溶解的氧气把亚硫酸氧化成硫酸;假设3:SO2中混有空气,把亚硫酸氧化成硫酸
⑶2SO2 +O2 +2H2O = 2H2SO4或SO2 +H2O =H2SO3、2H2SO3 + O2=2H2SO4;H2SO4 + BaCl2=
BaSO4↓+2HCl?
⑷BaCl2溶液中混有Ba(NO)3、HNO3、H2O2、Fe3+等均可
本题解析:
本题难度:一般
5、实验题 试用简单的实验证明,在醋酸溶液中存在着CH3COO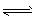 HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
参考答案:在醋酸溶液中滴入紫色的石蕊试液,溶液呈红色,再向上述溶液中加入少量醋酸铵固体,振荡后,溶液颜色变浅,说明 c(H+)变小,原因是加入的CH3COO -使平衡向左移动,由此说明醋酸溶液存在着醋酸的电离平衡。
本题解析:
本题难度:一般