1、选择题 某同学组装了如图所示的电化学装置电极I为Al,其他电极均为Cu,则

A.电流方向:电极IV→ →电极I
→电极I
B.电极I发生还原反应
C.电极II逐渐溶解
D.电极III的电极反应:Cu2++2e-==Cu
2、选择题 “ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是(?)
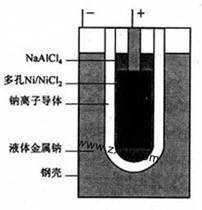
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为:NiCl2+2e-=Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
3、填空题 A、B、C、D、E、W均为短周期元素,原子序数依次增大。回答下列问题
(1)E单质为双原子分子,气体E的密度3.17g/L(标准状况),写出用石灰水吸收E反应的离子方程式:
___________________
(2)由A、B、D元素原子组成的化合物CH4和H2O在一定条件下发生反应:
CH4(g)+H2O(g) CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如图。
CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如图。
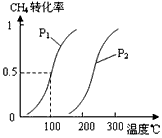
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为______________。
②图中的P1_______P2(填“<”、“>”或“=”),100℃时平衡常数为______________。
③在其它条件不变的情况下降低温度,逆反应速率将_______(填“增大”、“减小”或“不变”)
(3)由A、C、D元素原子组成的化合物N2H4和H2O2有广泛的用途。
①N2H4(肼)一空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的氢氧化钾溶液。电池放电时,负极的电极反应式为____________________。
②已知:16g液态N2H4(肼)与足量过氧化氢反应生成氮气和水蒸气,放出320.75KJ的热量。
H2O(1)=H2O(g) △H=+44 kJ・mol-1
2H2O2(1)=2H2O(1)+O2(g) △H=-196.4 kJ・mol-1
写出N2H4(肼)与氧气反应的热化学方程式为_____________________。
4、填空题 (1)P4(白磷,s)+5O2(g)
5、填空题 A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。

(1)A中反应的离子方程式为_____________________。
(2)B中Sn极的电极反应式为_____________________。
(3)C中被腐蚀的金属是____,总反应方程式为_____________________ 。比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________。