| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学试题《气体的净化、干燥、吸收与收集》高频试题强化练习(2020年最新版)(十)
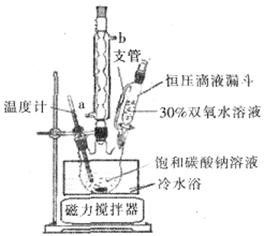
(3)在上述流程中,向反应前的H2O2中加入稳定剂的作用是____________________。 (4)该生产流程中可循环使用的物质是______________________________(填化学式)。 (5)生产过碳酸钠的流程中遗漏了一步,造成所得产品纯度偏低,请简述该步操作过程___________。 (6)实验室利用下图装置制备过碳酸钠,该装置中恒压滴液漏斗中支管的作用是_______,冷凝管应从__________处进水。 (7)由实验测定反应温度对产物的影响如下表:根据下表数据,你认为反应最佳的温度选择的范围是_______________。
 、 、参考答案:(1)ABC(3分) (2)NH3(2分) (3)防止双氧水分解(2分) (4)CO2(2分) 本题解析:(1)过碳酸钠(Na2CO3・3H2O2)具有Na2CO3和H2O2的双重性质,则A、FeCl3溶液能与碳酸钠反应,因此氯化铁也与过碳酸钠反应,A正确;B.H2S与双氧水发生氧化还原反应,则也与过碳酸钠发生氧化还原反应,B正确;C.稀硫酸与碳酸钠反应,因此也与过碳酸钠反应,C正确;D.NaHCO3溶液与碳酸钠以及双氧水等均不反应,因此也与过碳酸钠不反应,D不正确,答案选ABC。 本题难度:一般 4、选择题 除去CO中少量的CO2,选用的试剂和装置均正确的是( ) 参考答案:A、二氧化碳是酸性气体,能和碱液反应,一氧化碳和碱不反应,所以可用碱液洗气,故A正确; 本题解析: 本题难度:简单 5、实验题 (13分)下面是甲、乙、丙三位同学制取乙酸乙酯的过程。 参考答案:(13分) 1)催化剂 本题解析:略 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《物质的量》.. | |