|
高考化学知识点总结《化学反应与能量》试题预测(2020年最新版)(十)
2021-02-18 04:40:27
【 大 中 小】
|
1、选择题 根据键能数据估算CH4(g)+4F2(g) =CF4+4HF(g)的反应热ΔH为

[? ]
A.-1940 kJ ・ mol-1
B.1940 kJ ・ mol-1
C.-485 kJ ・ mol-1
D.485 kJ ・ mol-1
参考答案:A
本题解析:
本题难度:一般
2、选择题 反应A(g)+B(g)  C(g)+D(g)过程中的能量变化如图所示。下列判断中正确的是 C(g)+D(g)过程中的能量变化如图所示。下列判断中正确的是
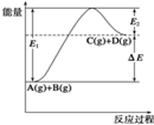
A.ΔE为活化能
B.加入催化剂后,E1、E2、ΔE均减小
C.反应物的总能量大于生成物的总能量
D.反应达到平衡时,升高温度,A的转化率增大
|
参考答案:D
本题解析:A、ΔE为反应热,不选A;B、加入催化剂后,E1、E2减小,但ΔE不变,不选B;C、反应物的总能量小于生成物的总能量,不选C;D、升温,反应向正向移动,A的转化率增大,选D。
考点:化学反应与能量的变化。
本题难度:一般
3、填空题 “温室效应”是哥本哈根气候变化大会研究的环境问题之一。CO2是目前大气中含量最高的一种温室气体。因此,控制和治理CO2是解决“温室效应”的有效途径。
(1)下列措施中,有利于降低大气中CO2浓度的有 (填字母)。
a.采用节能技术,减少化石燃料的用量 b.鼓励乘坐公交车出行,倡导低碳生活
c.利用太阳能、风能等新型能源替代化石燃料
(2)一种途径是将CO2转化成有机物实现碳循环。如:
2CO2(g)+2H2O(l)=C2H4(g)+3O2(g) △Hl="+1411.0" kJ/mol
2CO2(g)+3H2O(l)=C2H5OH(l)+3O2(g) △H2="+1366.8" kJ/mol
则由乙烯水化制乙醇的热化学方程式是 。
(3)在一定条件下,6H2(g)+2CO2(g) CH3CH2OH(g)+3H2O(g)。 CH3CH2OH(g)+3H2O(g)。

根据上表中数据分析:
①温度一定时,提高氢碳比[n(H2)/n(CO2)],CO2的转化率 (填“增大”“减小”或“不变”)。
②该反应的正反应为 (填“吸”或“放”)热反应。
参考答案:(1)abc(2分)(2)C2H4(g)+H2O(l)=C2H5OH(l) △H="-44.2" kJ/mol(2分)
(3)①增大(2分)②放(2分)
本题解析:(1)a.采用节能技术能减少化石燃料的使用,减少化石燃料的使用就减少了二氧化碳的排放,正确;b.化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;c.利用太阳能、风能能减少化石燃料的使用,化石燃料燃烧产物是二氧化碳,减少化石燃料的使用就减少了二氧化碳的排放,正确;故选abc。
(2)2CO2(g)+2H2O(l)
本题难度:困难
4、选择题 化学反应可以从多种角度认识和分析,下列对化学反应的认识错误的是( )
A.反应物中化学键断裂、生成物中化学键形成,同时伴随能量的变化
B.有电子转移的化学反应不一定能产生电流,但该反应一定为氧化还原反应
C.催化剂不能参与化学反应,但可以改变反应到达平衡的时间
D.同一化学反应往往可以采用不同的催化剂来改变化学反应速率
参考答案:A.化学反应的实质是旧化学键的断裂和新化学键的形成,在化学反应中常常伴随着能量的变化,故A正确;
B.构成原电池的氧化还原反应能产生电流,不能构成原电池的氧化还原反应不产生电流,但有电子转移的化学反应一定的氧化还原反应,故B正确;
C.催化剂参与化学反应,但最终能生成原物质,从表面看没有参加反应,实际上参加了化学反应,催化剂不能改变平衡移动,但能改变反应速率,所以可以改变反应到达平衡的时间,故C错误;
D.催化剂具有选择性和高效性,所以同一化学反应往往可以采用不同的催化剂来改变化学反应速率,故D正确;
故选C.
本题解析:
本题难度:简单
5、选择题 下列化合物中,既有离子键、又有共价键,且是非极性共价键的是( )
A.NaOH
B.Na2O2
C.H2O2
D.CaH2
参考答案:A.含离子键和O-H极性共价键,故A不选;
B.含离子键和O-O非极性共价键,故B选;
C.不含离子键,含O-H极性共价键和O-O非极性共价键,故C不选;
D.只含钙离子与H-之间的离子键,故D不选;
故选B.
本题解析:
本题难度:一般
|