1、简答题 有四组物质,它们的沸点(℃,P=1.01×105Pa)如下表所示:
| ① | He-268.8 | Ne-249.5 | Ar(x) | Kr-151.7
②
F2-187.0
Cl2-33.6
(a)58.7
I2-184.0
③
HF(Y)
HCl-84.0
HBr-67.0
HI-35.3
④
H2O(Z)
H2S-60.2
(b)-42.0
H2Te-1.8
|
试根据上表回答下列问题:
(1)物质b的分子式为:______,物质______(填a或b)易溶于苯.
(2)除极少数情况外,上述四种系列中物质的沸点与相对分子质量之间均存在一定的关系,该关系是______.
(3)上表中,______和______两种物质的沸点较同系列其它物质反常,反常的主要原因是______.
2、选择题 食盐晶体如下图所示。在晶体中,・表示Na+,o表示Cl-。已知食盐的密度为r g/cm3,NaCl摩尔质量M g/mol,阿伏加德罗常数为N,则在食盐晶体里Na+和Cl-的间距大约是

A.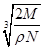 cm
cm
B.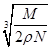 cm
cm
C.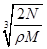 cm
cm
D.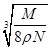 cm
cm
3、填空题 甲烷、甲醇、肼(N2H4)、氨和氢气等都可作为燃料电池的燃料。
(1)与甲醇互为等电子体的有机物分子式为:_________________, 甲醇的熔、沸点比甲烷的熔、沸点高,其主要原因是:______________________
(2)N2H4中N-N键键能__________(填“>”或“<” “=”) CH3CH3中C-C键键能,工业上将NH3或
(CH3)2CO与氯气反应后水解制取N2H4,(CH3)2CO中碳原子轨道的杂化类型为:_________、________,
1 mol(CH3)2CO中的π键数目为:_________。
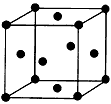
(3)用钛锰储氢合金储氢,与高压氢气钢瓶相比,具有重量轻、体积小的优点。锰原子外围电子排布式为:____________。金属钛的晶胞是面心立方结构(如图),则钛晶体的1个晶胞中钛原子数为:
________,钛原子的配位数为:________。
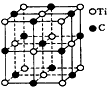
4、选择题 最近发现一种由钛(Ti)原子和碳原子构成的气态团簇分子,分子模型如图所示,其中圆圈表示钛原子,黑点表示碳原子,则它的化学式为
?[? ]
A.TiC
B.Ti13C14
C.Ti4C7
D.Ti14C13
5、填空题 如图所示,直线交点处的圆圈为NaCl晶体中Na+离子或Cl-离子所处的位置。这两种离子在空间三个互相垂直的方向上都是等距离排列的。
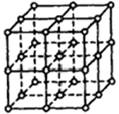
(1)晶体中,在每个Na+离子的周围与它最接近的且距离相等的Na+离子共有?个。
(2)已知食盐晶体的密度为2.2g/cm3,阿伏加德罗常数为6.02×1023mol-1。食盐晶体中两个距离最近的钠离子中心间的距离为?cm。计算过程如下:
?
?。
|