1、选择题 据报道1994年德国科学家利用数亿个镍原子(28Ni)对数亿个铅原子(82Pb)连续轰击数天后,制得一种新原子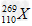 (暂用X表示),它属于一种新元素----110号元素,经分析它属于过渡元素。下列关于该元素的叙述中正确的是
(暂用X表示),它属于一种新元素----110号元素,经分析它属于过渡元素。下列关于该元素的叙述中正确的是
[? ]
A.这种原子(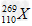 )的中子数为169
)的中子数为169
B.这种元素肯定是非金属元素
C.这种元素肯定是金属元素
D.这种元素属第三周期元素
参考答案:C
本题解析:
本题难度:简单
2、填空题 根据元素在周期表中的位置,回答下列有关问题:
(1)在1~18号元素中,非金属性最强的元素是______,金属性最强的元素是______.
(2)位于第三周期第VA族的元素的名称为______.
(3)C原子和O原子半径较大的是______.
参考答案:(1)在元素周期表中,非金属性最强的元素在周期表右上角、金属性最强的元素在周期表左下角,稀有气体除外,所以非金属性最强的元素是F、金属性最强的元素是Cs,故答案为:F;Cs;
(2)位于第三周期第VA族的元素的每个电子层上电子数分别为2、8、5,其核外电子数是15,元素原子序数与其原子核外电子数相等,该元素的原子序数是15,为磷元素,故答案为:磷;
(3)同一周期元素中,原子半径随着原子序数的增大而减小,C、O位于同一周期,且C的原子序数小于O,所以原子半径C的较大,故答案为:C.
本题解析:
本题难度:简单
3、简答题 元素周期表是学习化学的重要工具,它隐含着许多信息和规律.下面是八种短周期元素的相关信息(已知铍的原子半径为0.089nm)
| 元素代号 | A | B | C | D | E
原子半径/nm
0.160
0.143
0.102
0.099
0.074
主要化合价
+2
+3
+6,-2
-1
-2
|
F原子中无中子,G最高正价数与负价数相等,且最外层电子数是次外层的二倍,H元素单质焰色反应呈黄色
(1)B元素在元素周期表中的位置______.
(2)上述五种元素的最高价氧化物对应的水化物中酸性最强的是______(填化学式).
(3)用电子式表示A、D形成化合物的过程:______.
(4)H、E形成原子个数比为1:1的化合物为______(填化学式),含有的化学键类型为______.
(5)F与G形成的最简单的化合物的电子式______,该分子的空间构型为______.
(6)E的氢化物比C的氢化物的熔沸点高的原因是______.
(7)在有饱和食盐水的水槽中,用一倒扣在水槽中的试管用排饱和食盐水法先后收集等体积的GF4和D的单质气体,在光照条件下可观察到水槽中有晶体析出,试管内气体颜色逐渐变浅,液面上升,______,______等现象产生.
参考答案:F原子中无中子,所以是H,G最高正价数与负价数相等,是且最外层电子数是次外层的二倍,所以G是C,H元素单质焰色反应呈黄色,应为Na,A是Mg,B是Al,C是S,D是Cl,E是O.
(1)Al在周期表中位于第三周期第ⅢA族,故答案为:第三周期第ⅢA族;
(2)同周期从左到右最高价氧化物对应水化物的酸性逐渐增强,同主族从上到下最高价氧化物对应水化物的酸性逐渐逐渐减弱,所以酸性最强的在右上角,但是F没有正价,所以是HClO4,故答案为:HClO4;
(3)氯化镁是镁离子和氯离子之间通过离子键形成的离子化合物,其形成过程表示为:

,故答案为:

;
(4)H、E形成原子个数比为1:1的化合物为过氧化钠,过氧根中是非极性共价键,钠离子和过氧根之间是离子键,故答案为:Na2O2离子键和非极性键;
(5)F与G形成的最简单的化合物是甲烷,它的电子式为:
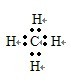
,空间结构是正四面体型,
故答案为:
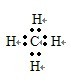
;正四面体;
(6)水的沸点高于硫化氢的沸点,因为水分子间存在氢键,故答案为:水分子间存在氢键;
(7)甲烷和氯气在光照的条件下生成的四种有机物均是难溶于水的,是油状液滴,氯化氢是极易溶于水的气体,溶于水形成盐酸液滴,而出现白雾,故答案为:试管壁出现油状液滴;试管中有少量白雾;
本题解析:
本题难度:一般
4、选择题 下列叙述正确的是( )
A.B、C、N元素最高化合价依次升高
B.P、S、Cl元素的单质与氢气化合逐渐变难
C.N、O、F元素原子半径依次增大
D.Li+、Na+、K+的还原性依次减弱
参考答案:A.B、C、N元素原子的最外层电子数分别为3、4、5,最正高化合价等于最外层电子数,故B、C、N元素最高化合价依次升高,故A正确;
B.同周期自左而右元素非金属性增强,非金属性越强,单质与氢气反应越容易,故P、S、Cl元素的单质与氢气化合逐渐容易,故B错误;
C.同周期自左而右原子半径减小,N、O、F元素原子半径依次减小,故C错误;
D.同主族自上而下金属性增强,金属性越强,阳离子的氧化性越弱,故Li+、Na+、K+的氧化性依次较弱,故D错误;
故选A.
本题解析:
本题难度:一般
5、选择题 据报道,法国里昂的科学家最近发现一种只由四个中子构成的粒子,这种粒子称为“四中子”,也有人称之为“零号元素”。下列有关“四中子”粒子的说法不正确的是
[? ]
A.该粒子不显电性
B.该粒子质量比氢原子大
C.该粒子质量数为4
D.在周期表中与氢元素占同一位置
参考答案:D
本题解析:
本题难度:简单