1��ѡ���� ���ڳ�����0.0lmol/L�İ�ˮ������������ȷ����
A��c(H+)+c(NH4+)=c(OH��)
B����������Ũ�ȵ��Ȼ����Һ���c(NH4+)+c(NH3�� H2O)="0.02" mol��L��1
C����������Ũ�ȵ������Ϻ�������Һ������
D����H2O�������c(H+)=1.0��10��12 mol��L��1
�ο��𰸣�AC
�����������ˮ��ֻ��һˮ�ϰ���ˮ�ǵ���ʣ��ֱ��ܲ��ֵ����笠����ӡ������Ӻ������������������ӣ�������Һ�ʵ����Ի����غ�ԭ��������Һ��c(OH��)=c(NH4+)+c(H+)����ȷ������Һ�������Ϊ1L������n=c?V������ǰһˮ�ϰ����Ȼ�淋����ʵ�������0.01mol��n(NH4+)+n(NH3��H2O)=0.01mol+0.01mol=0.02mol������ϡ��Һ���ܶȶ��ӽ���ˮ������ǰ����Ժ�����Һ����ı仯�����Ϻ���Һ�����Ϊ2L�����������غ�ԭ����֪�������Һ��n(NH4+)+n(NH3��H2O)=0.02mol������c=n/V����˻�Ϻ���Һ��c(NH4+)+c(NH3��H2O)=0.02mol/2L=0.01mol/L����B��������Һ�������Ϊ1L������n=c?V�����ǰһˮ�ϰ���HCl�����ʵ�����ȣ�����ʱ����ǡ����ȫ�кͣ��õ��Ȼ�狀�ˮ��NH4Cl��ǿ�������Σ�����ȫ�����笠������ܲ���ˮ�⣬�����Ȼ����Һ�����ԣ���C��ȷ�������⣬������c(NH3��H2O)=0.01mol/L��NH3��H2O�������������ʣ�����������c(OH��)<0.01mol/L������ˮ�ĵ���̶�ԶС��һˮ�ϰ�������Һ�е�c(OH��)<0.01mol/L��������Kw=1.0��10��14������Һ��c(H+)=Kw/c(OH��)>1.0��10��12 mol��L��1��������Һ�е�����������ˮ�ĵ��룬һˮ�ϰ����ܵ���������ӣ���ˮ�������c(H+)=��Һ��c(H+)=>1.0��10��12 mol��L��1����D����
�����Ѷȣ���
2�������
ij�¶��´�ˮ��C(H+) = 2��10-7 mol/L�����ʱ��Һ�е�C(OH-) = ___________��
���¶Ȳ��䣬����ϡ����ʹC(H+) = 5��10-6 mol/L�����ʱ��Һ�е�C(OH-) = ___________��
�ο��𰸣�
��ˮ�� C(OH-) = C(H+) = 2��10-7 mol/L? Kw = C(H+)��C(OH-) = 2��10-7��2��10-7 = 4��10-14?ϡ������ C(OH-) =" Kw" / C(H+) = (4��10-14) / (5��10-6) = 8��10-9 mol/L
�����������ˮ���������H+��OH-��ʼ����ȣ�֪��ˮ��C(H+) = C(OH-)�����ݴ�ˮ��C(H+) ��C(OH-)��������¶���ˮ��Kw��ֵ����Kw�����ʣ�ֻ���¶��йأ�������Ũ���أ������¶Ȳ��䣬ϡ������Kw��Ϊ��ֵ�����ô�ֵ����������е�C(OH-)��
�����Ѷȣ�һ��
3��ѡ���� ��֪�����£�0.1mol/L��һԪ��HA��Һ��pH��1��0.1mol/L��һԪ��MOH��Һ��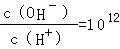 ������������Һ�������ϣ����ҹ�У�����Ũ�ȹ�ϵ����ȷ���ǣ�������
������������Һ�������ϣ����ҹ�У�����Ũ�ȹ�ϵ����ȷ���ǣ�������
A��c��OH����=c��HA��+c��H+��
B��c��M+����c��A������c��OH������c��H+��
C��c��A������c��M+����c��H+����c��OH����
D��c��M+��+c��H+��=c��A����+c��OH����
�ο��𰸣�C
���������0.1mol/L��һԪ��HA��Һ��pH��1�����Ჿ�ֵ��룬Ϊ���0.1mol/L��һԪ��MOH��Һ��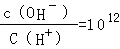 �����ˮ�����ӻ�����֪��
�����ˮ�����ӻ�����֪��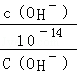 =1012������Һ������������Ũ��=0.1mol/L�����Լ�Ϊǿ����ߵ�������ʱǡ�÷�Ӧ����ǿ�������Σ������ε����ʼ�����غ�������
=1012������Һ������������Ũ��=0.1mol/L�����Լ�Ϊǿ����ߵ�������ʱǡ�÷�Ӧ����ǿ�������Σ������ε����ʼ�����غ�������
�⣺0.1mol/L��һԪ��HA��Һ��pH��1�����Ჿ�ֵ��룬Ϊ���0.1mol/L��һԪ��MOH��Һ��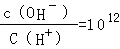 �����ˮ�����ӻ�����֪��
�����ˮ�����ӻ�����֪��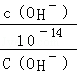 =1012������Һ������������Ũ��=0.1mol/L�����Լ�Ϊǿ����ߵ�������ʱǡ�÷�Ӧ����ǿ�������Σ�
=1012������Һ������������Ũ��=0.1mol/L�����Լ�Ϊǿ����ߵ�������ʱǡ�÷�Ӧ����ǿ�������Σ�
A�����������غ��c��OH����=c��HA��+c��H+������A��ȷ��
B������Һ���������Σ��Ҹ�����ǿ������������Һ�ʼ��ԣ���c��OH������c��H+�������ݵ���غ��c��M+����c��A����������Һ���������Ũ�ȴ�������������Ũ�ȣ����Ը���Һ������Ũ�ȴ�С˳����c��M+����c��A������c��OH������c��H+������B��ȷ��
C������Һ���������Σ��Ҹ�����ǿ������������Һ�ʼ��ԣ���c��OH������c��H+�������ݵ���غ��c��M+����c��A����������Һ���������Ũ�ȴ�������������Ũ�ȣ����Ը���Һ������Ũ�ȴ�С˳����c��M+����c��A������c��OH������c��H+������C����
D�����ݵ���غ��c��M+��+c��H+��=c��A����+c��OH��������D��ȷ��
��ѡ��C��
���������⿼���˻����Һ�����жϣ���ȷ�ж��ἰ���ǿ���ǽⱾ��ؼ��������Һ�е����ʼ�����غ���������ɣ��Ѷ��еȣ�
�����Ѷȣ�һ��
4��ѡ����
A��11��1
B��9��1
C��1��11
D��1��9
�ο��𰸣�D
�������������ȿɲ��ó�����㷨��Ҳ�ɲ��ù��㷨������֪�������������Ϊ1��10ʱ�����û��Һ��pH=7����pH=11,�Լ��ԣ��ʼ��������Ӧ����1��10����ѡD��
�����Ѷȣ�һ��
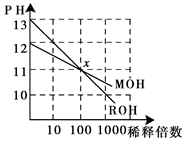
5��ѡ���� MOH��ROH����һԪ�����Һ�ֱ��ˮϡ��ʱ��pH�仯����ͼ��ʾ��������������ȷ����
 ?
?
A��ROH��һ������
B����x�㣬c(M��) �� c(R��)
C����x�㣬MOH��ȫ����
D��ϡ��ǰ��c(ROH) ��10 c(MOH)
�ο��𰸣�B
�����������ͼ���Կ�����ROHԭ����pHΪ13��ϡ��ʮ����pHΪ12��ϡ��һ�ٱ���pHΪ11���ɴ˿����жϣ�ROHΪǿ��෴MOHΪ�����A������x�㣬�������ʵ�pH��ȣ����ݵ���غ����֪����c(M��) �� c(R��)����B��ȷ��MOHΪ���������x�㣬MOH��Ȼ����ȫ���룬����C������ΪMOHΪ�����ROHΪǿ���Ȼϡ��ǿ��ROH��pHΪ13����MOH��pHΪ12������c(ROH)��Ϊ c(MOH)��10�㣬����D����
������������ͼ����ǿ����������Ǹ߿�������ȵ㣬������һ�����ۺ��ԣ������Ѷ����С�
�����Ѷȣ�һ��