1、选择题 一定条件下硝酸铵受热分解的未配平化学方程式为 NH4NO3 →HNO3 + N2 + H2O ,在反应中被氧化与被还原的氮原子数之比为?
[? ]
A. 5:3
B. 5:4
C. 1:1
D. 3:5
参考答案:A
本题解析:
本题难度:简单
2、选择题 废水中常含有卤代烃,研究发现,把铁粉放在废水中可以除去卤代烃,该过程的机理为:Fe+ RCH2X+ H+ →?RCH3+X-+Fe2+(X 为卤素)。下列说法中正确的是?
[? ]
A.处理后,废水的pH 减小
B.该反应是置换反应
C.反应过程中RCH2X 是氧化剂
D.处理含1 mol 卤代烃的废水时,转移1 mol 电子
参考答案:C
本题解析:
本题难度:一般
3、填空题 铜在自然界存在于多种矿石中,如

请回答下列问题:
(1)上表所列铜化合物中,铜的质量百分含量最高的是______________。
(2)工业上以黄铜矿为原料,采用火法熔炼工艺生产铜。该工艺的中间过程会发生反应:
2Cu2O+Cu2S 6Cu+SO2↑,反应的氧化剂是________。
6Cu+SO2↑,反应的氧化剂是________。
(3)SO2尾气直接排放到大气中造成环境污染的后果是____________________________;处理该尾气可得到有价值的化学品,写出其中1种酸和1种盐的名称______________。
(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。请简述粗铜电解得到精铜的原理:___________________________。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性及其有无因果关系的判断都正确的是________(填字母)。

参考答案:(1)Cu2S
(2)Cu2S和Cu2O
(3)形成酸雨,会对植物和建筑物等造成严重危害;硫酸、硫酸钠
(4)以硫酸铜-硫酸溶液为电解液,电解时,粗铜(阳极)中的铜以及比铜活泼的金属失去电子进入溶液,不如铜活泼的金属沉入电解槽形成“阳极泥”;溶液中的Cu2+得到电子沉积在纯铜(阴极)上。
(5)AD
本题解析:
本题难度:一般
4、选择题 下列变化中,需加入氧化剂才能实现的是
[? ]
A.CaCO3→CaO
B.CuO→Cu
C.Zn→ZnSO4
D.H2O(g)→H2O(l)
参考答案:C
本题解析:
本题难度:简单
5、选择题 LiAlH4(?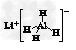 )、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125?℃分解为LiH、H2和Al。下列说法不正确的是
)、LiH既是金属储氢材料又是有机合成中的常用试剂,遇水均能剧烈分解释放出H2,LiAlH4在125?℃分解为LiH、H2和Al。下列说法不正确的是
[? ]
A.LiH与D2O反应,所得氢气的摩尔质量为4?g/mol
B.1?mol?LiAlH4在125?℃完全分解,转移3?mol电子
C.LiAlH4溶于适量水得到无色溶液,则化学方程式可表示为:LiAlH4+2H2O===LiAlO2+4H2↑
D.LiAlH4与乙醛作用生成乙醇,LiAlH4作还原剂
参考答案:A
本题解析:
本题难度:简单