1、选择题 下列溶液中各微粒的浓度关系正确的是( )
A.25℃时,物质的量浓度相等的Na2CO3和CH3COONa溶液的pH值:Na2CO3>CH3COONa
B.某二元弱酸的酸式盐NaHA溶液中:c(H+)+c(Na+)=c(OH-)+c(HA-)+c(A2-)
C.1.0mol/L?Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+c(H2CO3)
D.向氟化钠溶液中加入适量氢氟酸,得到的酸性混合溶液:c(F-)>c(Na+)>c(H+)>c(OH-)
参考答案:A.酸性:CH3COH>H2CO3,酸越弱,在强碱盐中酸根离子的水解程度越大,溶液碱性越强,则pH值:Na2CO3>CH3COONa,故A正确;
B.二元弱酸的酸式盐NaHA溶液遵循溶液电中性的原则,应有c(H+)+c(Na+)=c(OH-)+c(HA-)+2c(A2-),故B错误;
C.由H2O

H++OH-,可知溶液应遵循质子守恒:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故C错误;
D.向氟化钠溶液中加入适量氢氟酸,得到的酸性混合溶液,说明HF电离程度大于F-水解程度,存在c(F-)>c(Na+)>c(H+)>c(OH-),故D正确.
故选AD.
本题解析:
本题难度:一般
2、选择题 用0.10 mol・L-1的盐酸滴定0.10 mol・L-1的氨水,滴定过程中不可能出现的结果是?
[?]
A.
B.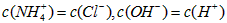
C.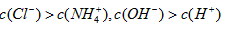
D.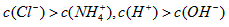
参考答案:A
本题解析:
本题难度:一般
3、选择题 25℃时,在20ml0.1mol・L-1NaOH溶液中逐滴加入0.2mol・L-1醋酸溶液,曲线如图所示,有关粒子浓度关系的比较中,不正确的是

[? ]
A.在A点:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
B.在B点:c(OH-)=c(H+),c(Na+)=c(CH3COO-)
C.在C点:c(CH3COO-)>c(Na+)>c(H+) >c(OH-)
D.在C点:c(CH3COO-)+c(CH3COOH)=2c(Na+)
参考答案:A
本题解析:
本题难度:一般
4、选择题 常温下,pH=11的氨水和pH=1的盐酸等体积混合后(不考虑混合后溶液体积的变化),恰好完全反应,则下列说法不正确的是?
[? ]
A.弱碱的浓度大于强酸的浓度
B.反应后的溶液呈酸性
C.原氨水中有1%的含氮粒子为NH4+
D.反应后的溶液中NH4+、NH3・H2O与NH3三种粒子的平衡浓度之和为0.05?mol/L
参考答案:A
本题解析:
本题难度:一般
5、填空题 已知:①25℃时弱电解质电离平衡数:Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13;难溶电解质的溶度积常数:Ksp(CaF2)=1.5×10-10 ②25℃时,2.0×10-3mol/L氢氟酸水溶液中,调节溶液pH(忽略体积变化),得到c(HF)、c(F-)与溶液pH的变化关系,如下图所示:
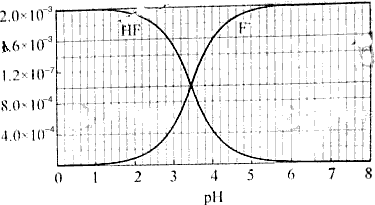 ?
? 
?图2
请根据以下信息回答下旬问题:
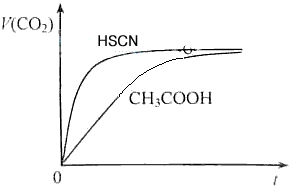
(1)25℃时,将20mL 0.10 mol/L CH3COOH溶液和20mL 0.10 mol/LHSCN溶液分别与20mL 0.10 mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)变化的示意图为图2所示:
①反应初始阶段,两种溶液产生CO2气体的速率存在明显差异的原因是 ___________________________________________________________________________________________________________,
②反应结束后所得两溶液中,c(CH3COO-)_______c(SCN-)(填“>”、“<”或“=”)
(2)25℃时,HF电离平衡常数的数值Ka≈ ,列式并说明得出该常数的理由 ________________________________________________________________________________________________________。
(3)4.0×10-3 mol/LHF溶液与4.0×10-4 mol/LCaCl2溶液等体积混合,调节混合液pH为4.0(忽略调节混合液体积的变化),通过列式计算说明是否有沉淀产生。
参考答案:(1)①相同的起始条件,只能是因为两种酸的电离度不同导致溶液中起始反应时H+浓度不同引起反应速率的不同。
②反应结束后,溶质为CH3COONa和NaSCN,因CH3COOH酸性弱于HSCN,故CH3COONa水解程度大,c(CH3COO-)<c(SCN-)。
(2)HF电离平衡常数Ka= c(H+)・c(F-)/ c(HF),其中c(H+)、 c(F-)、 c(HF)都是电离达到平衡时的浓度,选择中间段图像求解。根据图像:PH=4时,c(H+)=10-4, c(F-)=1.6×10-3、 c(HF)=4.0×10-4。Ka=0.4×10-3。
(3)PH=4.0,则c(H+)=10-4,此时:根据HF电离,产生的c(F-)=1.6×10-3,而溶液中的c(Ca2+)=2.0×10-4。c2(F-)×c(Ca2+)=5.12×10-10, 5.12×10-10大于Kap(CaF2)=1.5×10-10,此时有少量沉淀产生。
本题解析:
本题难度:一般