1、选择题 常温下,将amol/L的MOH(可溶性弱碱)与bmol/L的盐酸等体积混合,已知相同条件下MOH的电离程度大于M+的水解程度,则下列有关推论不正确的是?
[? ]
A.若混合后溶液的pH=7,则c(M+)=c(Cl-) ?
B.若a=2b,则c?(M+)?>?c(Cl-)?>?c?(MOH)?>?c(OH-)?>?c(H+) ?
C.若b=2a,则c(Cl-)?>?c(M+)?>?c(H+)?>?c(OH-)? ?
D.若混合后溶液满足c(H+)=c(OH-)+c(MOH),则可推出a=b
参考答案:C
本题解析:
本题难度:一般
2、选择题 下列有关电解质溶液中微粒的物质的量浓度关系不正确的是
[? ]
A.在0.1 mol.L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-)
B.在0.1 mol.L-1Na2CO3溶液中:c(OH -)-c(H+)=c(HCO3-)+2c(H2CO3)
C.向0.2 mol.L-1NaHCO3溶液中加入等体积0.1 mol.L-1NaOH溶液:c(CO32-)>c(HCO3-)> c(OH-)>c(H+)
D.常温下,pH =7的CH3 COONa和CH3 COOH的混合溶液:c(Na+)=c(CH3COO -)>c(H+) =c(OH -)
参考答案:C
本题解析:
本题难度:一般
3、选择题 已知常温下CH3COOH的电离平衡常数为Ka?,常温下,向20mL?0.1?mol/L CH3COOH溶液中逐滴加入0.1?mol/LNaOH溶液,其pH变化曲线如图所示(忽略温度变化)。下列说法中正确的是
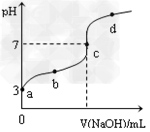
[? ]
A.?a点表示的溶液中由水电离出的H+浓度为1.0×10-3mol/L
B.?b点表示的溶液c(CH3COO-)<?c(Na+)
C.?c点表示CH3COOH和NaOH恰好反应完全
D.?b、d点表示的溶液中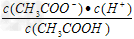 相等
相等
参考答案:D
本题解析:
本题难度:一般
4、选择题 下列实验操作都能达到预期目的是( )
①蒸干AlCl3溶液可得纯净的无水氯化铝;②可以采用多次盐析或多次渗析的方法分离、提纯蛋白质;③用广泛pH试纸测得某溶液pH为3.5;④滴入酚酞溶液确定纯碱中有无烧碱;⑤用米汤直接检验食用盐中是否含有碘元素;⑥用酸式滴定管量取20.00mL高锰酸钾酸性溶液;⑦用溴的四氯化碳溶液除去混在甲烷中的乙烯气体.
A.⑥⑦
B.②⑥
C.⑤⑥⑦
D.只有⑥
参考答案:B
本题解析:
本题难度:简单
5、选择题 下列各溶液中微粒的物质的量浓度关系不正确的是( )
A.10?mL?1?mol?L-1?NH4?C1溶液与5mL?0.2mol?L-1Na?OH溶液混合?c(Na+)=c(Cl-)>c(OH-)>c(H+)
B.0.1mol?L-1Na2S溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S)
C.只含有Na+、H+、Cl-、OH-的溶液中一定有:c(Cl-)=c(Na+)>c(H+)=c(OH-)
D.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3和NH4?C1三种溶液中:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4?C1)
参考答案:A、10?mL?1?mol?L-1?NH4?C1溶液与5mL?0.2mol?L-1Na?OH溶液混合后,恰好发生反应生成氯化钠和氨水,溶液显示碱性,c(OH-)>c(H+),氯化钠完全电离,所以c(Na+)=c(Cl-)>c(OH-)>c(H+),故A正确;
B、硫化钠溶液中存在质子守恒:c(OH-)=c(H+)+c(HS-)+2c(H2S),故B正确;
C、只含有Na+、H+、Cl-、OH-的溶液中的溶质的可能组成情况有:氯化钠和盐酸的混合物,c(Cl-)>c(Na+)>c(H+)>c(OH-);或者是氯化钠的水溶液,此时c(Na+)=c(Cl-)>c(OH-)=c(H+),还可以是氯化钠和氢氧化钠的混合物,此时c(Na+)>>c(OH-)>c(Cl-)>c(H+)等情况,故C错误;
D、(NH4)2SO4、(NH4)2CO3和NH4?C1三种溶液中,铵根离子的水解程度依次是:无影响、受促进,无影响,(NH4)2SO4、(NH4)2CO3中铵根离子浓度一定是大于等浓度的氯化铵中铵根离子浓度,即等浓度的三种溶液中,铵根离子浓度关系是(NH4)2SO4、>(NH4)2CO3>NH4?C1,当铵根离子浓度相等时,则c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4?C1),故D正确.
故选C.
本题解析:
本题难度:简单