1、选择题 一定温度下,可逆反应H2(g)+I2(g) 2HI(g)达到化学平衡状态的标志是(?)
2HI(g)达到化学平衡状态的标志是(?)
A.混合气体的压强不再变化
B.混合气体的颜色不再变化
C.反应速率v(H2)="0.5v" (HI)
D.c (H2):c(I2):c(HI)=1:1:2
参考答案:B
本题解析:判断一个反应是否达到平衡状态的实质是正逆反应速率相等,标志是所给条件是否从“变”达到“不变”。A该反应气体分子总数前后一样,故压强始终不变;B碘蒸气为紫色,随着反应的进行,容器内气体的颜色逐渐变浅;C反应速率之比始终与化学计量系数之比相等,故不能用于判断反应是否达到平衡状态;D各物质的浓度之比与化学计量系数之比相同, 与反应是否达到平衡无关系。故答案选B。
点评:判断一个反应是否达到平衡状态,是历年高考的重点。考生在备考过程中应抓住实质、通过标志进行分析。难度中等,一般以选择题出现。
本题难度:一般
2、选择题 在体积相同的A、B两个带活塞的玻璃容器中,分别注入1/4体积颜色相同的NO2与溴蒸气,然后将活塞同时向外拉出到1/2(快速),过一会可以看到
A、A中的颜色比B中的浅? B、A中的颜色比B中的深
C、A中的颜色与B中的深浅相同? D、A中颜色比开始时深
参考答案:B
本题解析:两种气体的变化情况不一样,对于Br2(g)只是物理变化,对于NO2(g)是一个平衡移动的过程2NO2?N2O4,相当于压强减小,相当于压强减小,物理变化使之颜色变浅,但随之平衡又向生成NO2方向移动。故选B。
点评:对气体参加的反应,体积对应的就是浓度,也就是浓度影响;
只是反应在一定体积的容器中进行,因此反应物和产物所占据的体积是相同的,也就是浓度的改变幅度是相同的。
如果体积减小,则化学平衡朝气体分子数减少的方向移动;
反之,如果体积增大,则化学平衡朝气体分子数增大的方向移动。
本题难度:简单
3、选择题 在恒容的密闭容器中,下列反应分别达到平衡后,有关说法正确的是
A.2HI(g) H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大
H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大
B.2NO2(g) N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅
N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅
C.2SO2(g)+O2(g) 2SO3(g);DH<0,升温后,平均相对分子质量减小
2SO3(g);DH<0,升温后,平均相对分子质量减小
D.3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加
Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加
参考答案:C
本题解析:考查了勒夏特列原理的相关内容
A:降温,平衡正向移动,碘蒸气浓度增大,颜色加深,但气体总物质的量不变,压强不变
B:在恒容状态下,充入氩气,虽体系压强增大,但各物质的浓度不变,对反应无任何影响。
C:升温,平衡逆向移动,气体的总物质的量增大,而质量不变,故平均相对分子质量减小。
D:铁为固体,不会影响反应。
故答案为C
本题难度:简单
4、填空题 (10分)向2 L的密闭容器中加入一定量的A、B、C三种气体,一定条件下发生反应,各物质的物质的量随时间变化如图甲所示。图乙为t2时刻后改变条件平衡体系中反应速率随时间变化的情况,且4个阶段所改变的外界条件均不相同,已知t3――t4阶段为使用催化剂。观察下图,回答下列问题:
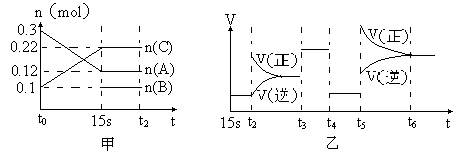
(1)甲图中从反应至达到平衡状态,生成物C的平均反应速率为?。
(2)乙图中t2时引起平衡移动的条件是?,t5时引起平衡移动的条件是?。
(3)乙图中表示平衡混合物中,在这4个阶段中C的含量最高的一段时间是?。
(4)该反应的化学方程式可以表示为:?,正反应为?(填“放热”或“吸热”)反应。
(5)反应开始时加入的B的物质的量为?。
参考答案:(1)? 0.004? mol/Ls?(2分)。
(2)?增加A的浓度,升高温度。(3)t5――t6。(每空1分)
(4) 3A(g) B(g)+2C(g),(2分)吸热(1分)
B(g)+2C(g),(2分)吸热(1分)
(5)0.04mol(2分)
本题解析:略
本题难度:一般
5、填空题 在一个固定体积的密闭容器中,向容器中充入2 mol A 和1 mol B,发生如下反应:2A(g) + B(g)  3C(g) + D(s),反应达到平衡时C的浓度为1.2 mol/L.
3C(g) + D(s),反应达到平衡时C的浓度为1.2 mol/L.
(1)若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,则正反应为________(填“吸热”或“放热”)反应.
(2)若维持容器体积和温度不变,按下列方法加入起始物质,达到平衡时C的浓度仍为1.2 mol/L的是______(用序号填空).
①4 mol A+2 mol B ②3 mol C+1 mol D+l mol B
③3 mol C+2 mol D ④1.6 mol A+0.8 mol B+0.6 mol C
(3)某温度下,向容器中加入3 mol C和0.8 mol D,反应达到平衡时C的浓度仍为1.2 mol/L,则容器的容积V应大于________L,小于________L.
参考答案:(4分) (1)吸热(1分) (2)③(1分) (3)0.5 2.5(2分)
本题解析:(1)根据方程式可知,反应前后体积不变,但气体的质量减小。所以若使容器温度升高,平衡时混合气体的平均相对摩尔质量减小,这说明升高温度,平衡向正反应方向移动,即正方应是吸热反应。
(2)维持容器体积和温度不变,达到平衡时C的浓度仍为1.2mol/L,为等效平衡,且为完全等效平衡,按化学计量数转化到左边满足2molA和1molB即可,由2A(g)+B(g) 3C(g)+D(S)可知:
3C(g)+D(S)可知:
①4molA+2molB与初始A、B的物质的量不同,故①错误;
②3molC+lmolD+1molB换算成A、B,A、B物质的量分别为2mol、2mol,与初始A、B的物质的量不同,故②错误;
③3molC+2molD?换算成A、B,A、B物质的量分别为2mol、1mol,D为1mol,D是固体,对平衡无影响,故③正确;
④1.6mol?A+0.8mol?B+0.6molC换算成A、B,没有D,C不能反应,与初始A、B的物质的量不相同,故④错误,答案选③。
(3)若C未转化时,C的物质的量为3mol,此时体积最大,所以容器的体积V=3mol÷1.2mol/L=2.5L;若D完全反应时,平衡时C的物质的量最小,此时体积最小,根据方程式计算反应的C的物质的量:
2A(g)+B(g)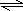 3C(g)+D(S)
3C(g)+D(S)
2.4mol?0.8mol
所以C的物质的量最小为3mol-2.4mol=0.6mol
所以容器的体积V=0.6mol÷1.2mol/L=0.5L
点评:该题是高考中的常见题型,属于中等难度试题的考查,侧重对学生分析、归纳和总结问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。采用极限反应法是解(3)题的关键,采用极限反应法求出C的物质的量,从而求出容器体积范围。
本题难度:困难