1��ѡ���� ����ȼ�ϵ�������ں���ɻ��������Բ����缫��KOH��Һ������ʣ�������������ȷ����
[? ]
A��H2�ڸ�������������Ӧ ����
B��ȼ�ϵ�ص�����ת���ʿɴ�100% ����
C������Ϊ����Ⱦ��ˮ�����ڻ����Ѻõ�ء���
D������ʱ���ܷ�ӦΪ��2H2+ O2= 2H2O
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� �鴦�ƺ��ʻ���õġ���Яʽ�Ҵ������ǡ���ȼ�ϵ��Ϊ����ԭ���������Ի����У��������Ҵ����Ա���ȫ����ΪCO2����ʵ���Ҵ�������ΪX������һ���缫�ķ�ӦʽΪ��
CH3CH2OH��2e-��X+2H+������˵������ȷ����
[? ]
A������ܷ�ӦΪ��2CH3CH2OH+O2��2CH3CHO+2H2O
B����һ���ĵ缫��ӦʽΪ��O2?+?4e-?+?2H2O?=?4OH-
C���Ҵ�������������Ӧ�����Ӿ������·����
D������ڲ�H+���������ƶ�
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� Ŀǰ����ѧ�������о�����һ�ָ��ܵ��--�����أ����������ơ���Ϊ�������Ե���Ħ�-Al2O3�մ����������ʣ���Ӧʽ���£�2Na+xS?Na2Sx������˵����ȷ���ǣ�������
A���ŵ�ʱ��Na��������S��������ԭ��Ӧ
B�����ʱ���Ƽ������Դ����������
C���ŵ�ʱ�����������ķ�ӦΪ��S
-2e=xS
D�����ô˵�ص��AgNO3��Һ��������������״���µ�����1.12Lʱ�����ĵĽ�����Ϊ4.6g
�ο��𰸣�A���ڷŵ�ʱ�����ʵõ��ӣ�����������ʧ���ӣ�����������A����
B�����ʱ���Ƽ������Դ�ĸ����������������Դ��������������B����
C���ŵ�ʱ����ԭ��ط�Ӧ��������ӦΪ��xS+2e-=Sx2-����C����
D�����AgNO3��Һʱ������������1.12L����������壬����0.05mol��������������4OH--4e-=O2��+2H2O������0.05mol����ת�Ƶ���Ϊ0.2mol�����������طŵ�ʱ�ĸ�����Ӧ��2Na-2e-=2Na+��������Ľ�����0.2mol����4.6g����D��ȷ��
��ѡD��
���������
�����Ѷȣ���
4��ѡ���� Ǧ�����ǵ��͵Ŀɳ���أ����ִ����������Ź㷺��Ӧ�ã����硢�ŵ簴��ʽ���У�
Pb+PbO2+2H2SO4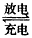 2PbSO4+2H2O���йظõ�ص�˵����ȷ����
2PbSO4+2H2O���йظõ�ص�˵����ȷ����
[? ]
A. �ŵ�ʱ�������ڵ�·��H+���ƶ�
B. �ŵ�ʱ��ÿͨ��1 mol���ӣ����ؾ�Ҫ����2 mol H2SO4
C. ���ʱ��������Ӧ��PbSO4+2e-=Pb+SO42-
D. ���ʱ��Ǧ���صĸ�������ӵ�Դ�ĸ�������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
5��ѡ���� ��10�֣��о�NO2��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣
��1�����÷�Ӧ6NO2�� 8NH3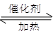 7N2��12 H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������?L��
7N2��12 H2O�ɴ���NO2����ת��1.2mol����ʱ�����ĵ�NO2�ڱ�״������?L��
��2����֪��2SO2��g��+O2��g��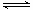 2SO3��g��?��H=��196.6 kJ��mol-1
2SO3��g��?��H=��196.6 kJ��mol-1
2NO��g��+O2��g��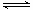 2NO2��g��?��H=��113.0 kJ��mol-1
2NO2��g��?��H=��113.0 kJ��mol-1
��ӦNO2��g��+SO2��g��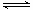 SO3��g��+NO��g���Ħ�H=?kJ��mol-1��
SO3��g��+NO��g���Ħ�H=?kJ��mol-1��
��3�����������ֳư�������أ��ŵ�ʱ���ܷ�ӦΪ��Fe+Ni2O3+3H2O= Fe(OH)2+2Ni(OH)2
����طŵ�ʱ�������缫��ӦʽΪ?��
�ο��𰸣�����10�֣�
��1��6.72��3�֣�
��2��- 41.8��3�֣�
��3��Ni2O3+3H2O+2e-=2Ni��OH��2+2OH-��4�֣�
���������
��NO2�ڱ�״����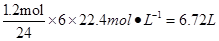
�Ƣ�2SO2��g��+O2��g��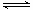 2SO3��g��?��H=��196.6 kJ��mol-1
2SO3��g��?��H=��196.6 kJ��mol-1
��2NO��g��+O2��g��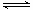 2NO2��g��?��H=��113.0 kJ��mol-1
2NO2��g��?��H=��113.0 kJ��mol-1
���٨D�ڣ���2�ã�����196.6 kJ��mol-1+113.0 kJ��mol-1����2=- 41.8 kJ��mol-1
�ǣ�Ni2O3+3H2O+2e-=2Ni��OH��2+2OH-
�����Ѷȣ�һ��