范德华力
参考答案:B
本题解析:干冰晶体中分子之间的作用力是范德华力。
本题难度:一般
2、选择题 氢叠氮酸(HN3)与醋酸性质相近,其盐稳定,但受撞击时易迅速发生反应,生成氮气。关于氢叠氮酸以下说法:①NaN3的水溶液呈碱性 ②固体HN3属分子晶体 ③固体NaN3属离子化合物 ④NaN3可用于小汽车防撞保护气囊,其中正确的是
A.①②③④
B.①②③
C.②③④
D.①③④
参考答案:A
本题解析:
叠氮酸与醋酸性质相近,应为弱酸,则其强碱盐能水解呈碱性,说法①正确。HN3是气态氢化物,其固体应属于分子晶体,说法②正确。NaN3是碱金属形成的盐,应属于离子晶体,说法③正确。NaN3通常条件下稳定,只是在受撞击时才迅速发生反应释放出无毒的氮气,能满足由小汽车撞击后迅速产生无毒且不易燃的气体的要求,能满足非撞击条件下安全的要求,因而可用于小汽车防撞气囊,说法④正确。
本题难度:一般
3、选择题 最近,美国Lawrece Liermore国家实验室(LINL)的V・Lota・C・S・Yoo和H・cynn成功地在高压下将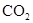 转化为具有类似 转化为具有类似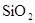 结构的原子晶体,下列关于 结构的原子晶体,下列关于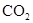 的原子晶体说法,正确的是( ) 的原子晶体说法,正确的是( )
A.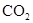 的原子晶体和分子晶体互为同分异构体 的原子晶体和分子晶体互为同分异构体
B.在一定条件下,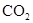 原子晶体转化为分子晶体是物理变化 原子晶体转化为分子晶体是物理变化
C.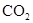 的原子晶体和 的原子晶体和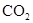 分子晶体具有相同的物理性质和化学性质 分子晶体具有相同的物理性质和化学性质
D.在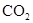 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合 的原子晶体中,每一个C原子周围结合4个O原子,每一个O原子跟两个C原子相结合
参考答案:D
本题解析:同分异构体的研究对象一般是单质;CO2的不同晶体类型之间的转变过程中,化学键发生了改变,故为化学变化;CO2的不同晶体具有不同的物理性质;CO2的原子晶体结构类似于SiO2,故每个碳原子结合4个氧原子,每个氧原子结合2个碳原子。所以正确的答案选D。
本题难度:一般
4、选择题 下列物质的熔点高低顺序,正确的是
A.金刚石>晶体硅>碳化硅
B.K>Na
C.NaF<NaCl<NaBr
D.CI4>CBr4
参考答案:D
本题解析:
A.原子晶体熔点,比较共价键键长,键长越短,键能越大,物质越稳定;键长:C-C<C-Si<Si-Si,熔点:金刚石>碳化硅>晶体硅;
B.金属晶体键能的大小比较看金属原子的半径大小 ,半径越小 键能越大,熔点越高。K<Na
C.离子晶体熔点,比较晶格能,离子半径越小,所带电荷越多,晶格能越大,离子晶体熔点越高;离子半径:F-<Cl-<Br-,熔点:NaF>NaCl>NaBr ;
D.分子晶体熔点,比较分子间作用力,相对分子质量越大,分子间作用力越大,熔点越高。
【考点定位】比较物质的熔点和沸点的高低,通常按下列步骤进行,首先比较物质的晶体类型,然后再根据同类晶体中晶体微粒间作用力大小,比较物质熔点和沸点的高低,具体比较如下:
一、判断所给物质的晶体类型,然后按晶体的熔点和沸点的高低进行比较,一般来说晶体的熔点和沸点的高低是:原子晶体>离子晶体>分子晶体,例如:晶体硅>氯化钠>干冰。但并不是所有这三种晶体的熔点和沸点都符合该规律,例如:氧化镁(离子晶体)>晶体硅(原子晶体)。而金属晶体的熔点和沸点变化太大,例如汞、铷、铯、钾等的熔点和沸点都很低,钨、铼、锇等的熔点和沸点却很高,所以不能和其它晶体进行简单的比较。
本题难度:一般
5、填空题 如图所示的晶体结构是一种具有优良压电、铁电、电光等功能的晶体材料的晶胞。
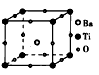
(1)晶体内与每个“Ti”紧邻的O原子数为_______个。
(2)晶体内与每个“Ba”紧邻的O原子数为_______个。
(3)晶体的化学式为________。
A.BaTiO8O12
B.BaTi4O8
C.BaTiO3
D.BaTi2O3
参考答案:(1)6
(2)12
(3)C
本题解析:
本题难度:一般
|