1�������� ���������ĵ���A��B���ֱ�ʢ��AgNO3��Һ��NaCl��Һ���ö��Ե缫���е�⣬��B�ص��������ռ���2��24 L(��״��)����ʱ����A�ص��������������ʶ��ٿˣ���������Һ����2 L��������Һ��pH���Ƕ��٣�
�ο��𰸣�1��6 g? 1? 13
���������A��B���ط����ķ�Ӧ�ֱ��ǣ�
A��4AgNO3+2H2O 4Ag+O2��+4HNO3
4Ag+O2��+4HNO3
B��2NaCl+2H2O 2NaOH+H2��+Cl2��
2NaOH+H2��+Cl2��
B����������H2 2��24 L����״�������൱��0��1 mol����·��Ӧ��0��2 mol����ת�ơ�1 mol����Ӧ����1 mol����0��5 mol Cl2��0��5 mol H2,0��25 mol O2��
��A����������O2Ϊ0��25 mol/1 mol��0��2 mol��32 g��mol-1=1��6 g,A���в���0��2 mol H+����Һ��pH=-lg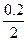 =1��
=1��
B��������0��2 mol OH-,��Һ��pH=-lg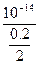 =13��
=13��
�����Ѷȣ���
2������� ��1��ij��ѧ��ȤС��ͨ��ʵ����ʵ�ֵ���ת���ɻ�ѧ�ܣ�������U�ι��м������������Ȼ�ͭ��Һ����ʯī�����缫����ֱͨ����Դ��ʼʵ�飮
�����Դ�����������ǵ��ص�______�����ü������ĵ缫��ӦʽΪ______������ü��ϲ����ʵ�鷽����������______��
�ڵ�ⷴӦ�Ļ�ѧ����ʽΪ______��
��2��ijѧ�����ֵ�Ͳʹ�õĸɵ�ء�С���ݺ�ʯī�缫�����ߵ��������������Ȼ��Ƶĵ�����ʵ�飬����ʯī�缫���������Ȼ��ƾ�����ʱ������û����������ʯī�缫�������ڵ��Ȼ�����ʱ���������ˣ��ɴ����ܵõ�������______��������Щ���۵Ľ�����______��
�ο��𰸣���1������ʯī�����缫��ⱥ���Ȼ�ͭ��Һ�����Դ��������������������������ʧ���ӷ���������Ӧ����������� ��ӦΪ��2Cl--2e-�TCl2�������������ķ�������ʪ��ĵ��۵⻯����ֽ���ڸõ缫����������֤�����ɵ���������
�ʴ�Ϊ������2Cl--2e-�TCl2������ʪ��ĵ��۵⻯����ֽ���ڸü�U�ιܿڸ�������ֽ������
�ڵ���Ȼ�ͭ����������ͭ����ط�ӦΪ��CuCl2??ͨ��?.??Cu+Cl2�����ʴ�Ϊ��CuCl2?ͨ��?.? Cu+Cl2����
��2����ʯī�缫���������Ȼ��ƾ�����ʱ������û����������ʯī�缫�������ڵ��Ȼ�����ʱ���������ˣ�����Ľ��ۣ������ڵ��Ȼ����ܵ��磬����Ϊ���ڵ��Ȼ������������ƶ��Ĵ��������������ɣ��������ֻ���������ӡ������ӣ������ڵ��Ȼ��Ʋ��ܵ��磬��������Ȼ��ƾ��岻�ܵ��磬����Ϊ�ڸ�����Ȼ��ƾ�������������������֮����ǿ�ҵ�����ö����������ƶ���
�ʴ�Ϊ�������ڵ��Ȼ����ܵ��硢�����ڵ��Ȼ��Ʋ��ܵ��磬��������Ȼ��ƾ��岻�ܵ��磻���ۢ�����Ϊ���ڵ��Ȼ������������ƶ��Ĵ��������������ɣ��������ֻ���������ӡ������ӡ����ۢ�����Ϊ�ڸ�����Ȼ��ƾ�������������������֮����ǿ�ҵ�����ö����������ƶ���
���������
�����Ѷȣ�һ��
3��ѡ���� �õ�ⷨ��ȡ�Ȼ�ͭ��Һ�е�ͭ��������ȷ���ǣ�������
A����ͭƬ���ӵ�Դ����������һ�缫�ò�Ƭ
B����̼�����ӵ�Դ����������һ�缫��ͭƬ
C��������������Һ������������
D���ô����ǵ�ľ��������������
�ο��𰸣�A���õ�ⷨ��ȡ�Ȼ�ͭ��Һ�е�ͭʱ��ͭ�������������������Դﵽ����ͭ��Ŀ�ģ���A����
B�����ʱ��������ͭ����Ե缫��̼��������ͭӦ����������B��ȷ��
C����������Ϊͭ��������������Һ����Ӧ����C����
D����������Ϊ�����������ô����ǵ�ľ�����飬���߲���Ӧ����D����
��ѡB��
���������
�����Ѷȣ���
4��ѡ���� ��ͼ������˫Һԭ���װ�á���ͼ���ж�����˵���������(����)
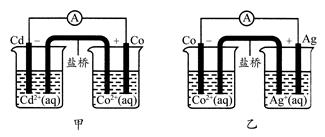
A����ͼ��ط�Ӧ�����ӷ���ʽΪ��Cd(s)��Co2��(aq)=Co(s)��Cd2��(aq)
B��2Ag(s)��Cd2��(aq)=Cd(s)��2Ag��(aq)��Ӧ�ܹ�����
C�����ŵ��������γɱպϻ�·����ʹ������Һ���ֵ�����
D����ͼ����1 mol����ͨ�����·ʱ��������108 g Ag����
�ο��𰸣�B
���������ԭ��ؼ����ķ�Ӧ�����ӷ���ʽΪCd��Co2��=Cd2����Co��Cd���������������Cd>Co��ԭ����ҷ����ķ�Ӧ����ʽΪCo��2Ag��=2Ag��Co2����Co���������������Co>Ag����ӦB���ܷ�����B�����ݵ����غ㣬1 mol e��ǡ��ʹ1 mol Ag��������D��ȷ��
�����Ѷȣ�һ��
5��ѡ���� iphone�ֻ�ʹ�õ�﮵���������ᡢ�����߶����ܹ�ע��Ŀǰ�ѳɹ����Ƴ�����﮵�ء�ij��﮵�ص��ܷ�Ӧʽ��Li��MnO2?��?LiMnO2������˵����ȷ����?
[? ]
A��MnO2�Ǹ������缫��ӦΪMnO2��e-��MnO2-
B����ع���ʱ������������ͨ�����·����
C������ڲ�������MnO2-��﮵缫�ƶ�
D���Ʊ�﮸����ã���ͬ�����������缫����ṩ�ĵ��ܸ��ࡣ
�ο��𰸣�C
���������
�����Ѷȣ�һ��