1��ѡ���� ʵ�����о���ѧ�Ļ�������ͼ����ʾ��ʵ�鷽����װ�û������ȫ��ȷ����
[? ]
A��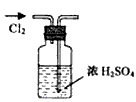 ����Cl2
����Cl2
B��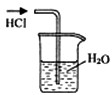 ����HCl
����HCl
C��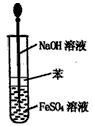 ��ȡFe(OH)2����
��ȡFe(OH)2����
D�� ϡ��ŨH2SO4
ϡ��ŨH2SO4
2��ʵ���� ijУ��ѧС��ѧ��������ͼ����װ�ý��С�����ˮ��Ӧ����ʵ�飬������������һ����ȡFeCl3��6H2O���壨ͼ�мгּ�β������װ�þ�����ȥ����

(1)װ��B�з�����Ӧ�Ļ�ѧ����ʽΪ____ ��
(2)װ��E�е�������____ ��
(3)ֹͣ��Ӧ����B����ȴ��ȡ���еĹ��壬�������ϡ�����ַ�Ӧ������Һ�ֳ����ݣ��ֱ������Һ�еĽ��������ӡ�����Fe3+���õ��Լ�Ϊ___ ����Fe2+���õ��Լ�Ϊ___��
(4)��С��ѧ������������Һ��ȡFeCl3��6H2O���壬�����������
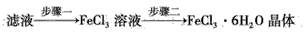
�ٲ���һ��ͨ������Cl2������Ӧ�����ӷ���ʽΪ___��
�ڲ������FeCl3��Һ�еõ�FeCl3��6H2O�������Ҫ�������£�����HCl�����н��У��� ������Ũ������ȴ���ᾧ�����ˡ�ϴ�ӡ����� ���������н���������Ũ������ʱ����____ʱ��Ӧֹͣ���ȡ��˹���Ӧ�������������ԭ����___�������ӷ���ʽ��ʾ����
(5) FeCl3��Һ��������Ȼ������д��FeCl3��Һ����Ȼ���е�H2S��Ӧ�����ӷ���ʽ��____��
3��ʵ���� TiO2��Ϳ�ϡ��������ױƷ���������ż���㷺��Ӧ�á�ijѧϰС��ͬѧ��ʵ������������(��Ҫ�ɷ�ΪFeTiO3������SiO2������)ģ�ҵ����TiO2��?�����������
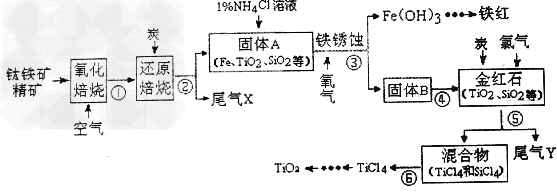
�ش��������⣺
(1)ѡ���Ҫ��װ���Ʊ����ռ��������������������������װ�õ���ȷ����˳��Ϊ_________________?(�������ӿڵ���ĸ���)�����װ��E�����ԵIJ�������Ϊ___________��
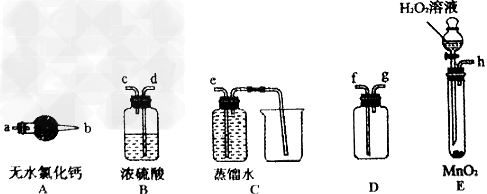
(2)������������绯ѧ��ʴ�Ĺ����У�O2������缫��Ӧ�⣬����������һ����ѧ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_________________
(3)�������й���B����ϴ�ӵõ����ʯ����֤���ʯCl�C��ϴ����ʵ�鷽����____________
(4)������в�����β��Y�к�������Cl2����Ⱦ���������п���������Cl2���Լ�Ϊ_______(����ĸ���)?��
a������ʳ��ˮ?b��Ũ����?c��ŨNaOH��Һ?d��ʯ����
(5)�����±����ݣ�������з���TiCl4��SiCl4�����IJ�������Ϊ_______�����õ�����Ҫ�����������ƾ��ơ��¶ȼ����________________��
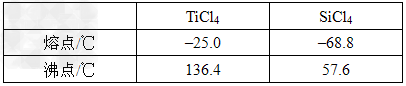
4������� ʵ������������������Ʊ��������������й����ʵ�����������±���
| ������ | ��Է������� | �ܶ�/g-cm-3 | �е�/�� | �ܽ��/100gˮ
������
74
0.80
118.0
9
������
60
1.045
118.1
����
����������
116
0.882
126.1
0.7
|
��ش��й����⣮
I�����������ֲ�Ʒ���Ʊ�
������Բ����ƿ��װ���ʯ������18.5mL��������15.4mL�����ᣨ�Թ��������ټ�3��4��Ũ���ᣮȻ��װ��ˮ�������ã�ʵ������в��Ϸ����ȥ��Ӧ���ɵ�ˮ�����¶ȼƼ����������ܣ���������������Ӧ��
��1����ʵ������п��ܲ��������л��������д������һ�ֵĽṹ��ʽ______��
��2����Ӧʱ����������������IJ��ʣ���ʵ�鷢���¶ȹ������IJ��ʷ������ͣ����ܵ�ԭ����______��
�������������ֲ�Ʒ���Ʊ�
��1����Բ����ƿ�е�Һ��ת���Һ©���У����ñ���Na2CO3��Һϴ���л��㣬�ò�������Ŀ����______��
��2�������������ͼ1��ʾװ������
��ͼ2������A��B�����Ʒֱ�Ϊ______��
�������ռ�������������Ʒʱ��Ӧ���¶ȿ�����______���ң�
��������
�����Ƶõ�����������������Ϊ13.92g���������������IJ���Ϊ______��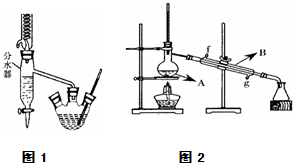
5��ʵ���� ����Fe(OH)2���ױ�����������ʵ���Һ�������������Һ���ռӦ�Ƶð�ɫ������Fe(OH)2������Ӧ����ͼ��ʾ���ʵ������Ƶð�ɫ�Ĵ�����Fe(OH)2���������缫���Ϸֱ�Ϊʯī������
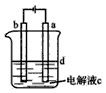
(1)a�缫����ӦΪ____���缫��ӦʽΪ____��
(2)���Һc������________��
A������ˮ
B��NaCl��Һ
C��NaOH��Һ
D��CuCl2��Һ
(3)dΪ������������____���ڼ��뱽֮ǰ��CӦ���μ���____��
(4)Ϊ���ڽ϶�ʱ���ڿ�����ɫ�������ɲ�ȡ�Ĵ�ʩ��____��
A������ϡ���������Һ
B���ʵ������Դ�ĵ�ѹ
C���ʵ���С���缫�����
D���ʵ����͵��Һ���¶�
(5)��C����Na2SO4��Һ�������һ��ʱ�俴����ɫFe(OH)2�������ٷ��ӵ�Դ��⣬���˵缫�Ͽ����� ���⣬���������һ��������Ϊ____��