1、填空题 (18分)现有反应:mA(g)+nB(g) pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
(1)该反应的逆反应为_________热反应,且m+n_________p(填“>”“=”“<”)。
(2)减压时,A的质量分数_________。(填“增大”“减小”或“不变”,下同)
(3)若加入B(体积不变),则A的转化率_________,B的转化率_________。
(4)若升高温度,则平衡时B、C的浓度之比将_________。
(5)若加入催化剂,平衡时气体混合物的总物质的量_________。
(6)若B是有色物质,A、C均无色,则加入C(体积不变)时混合物颜色_______,而维持容器内压强不变,充入氖气时,混合物颜色_______(填“变深”“变浅”或“不变”)。
参考答案:(18分)每空2分
(1)放,大于 (2)增大(3)大,小(4)小(5)不变(6)深,变浅
本题解析:略
本题难度:一般
2、选择题 将2molS02和1molO2放入一个密闭容器中,在一定的条件下反应到达“平衡状态”,此时,下列所示容器内存在各物质的物质的量中,一定不可能的是
A.0mol S02
B.1mol S02
C.2mol S03
D.0.3mol O2
参考答案:AC
本题解析:略
本题难度:简单
3、选择题 将一定量纯净的氨基甲酸铵置于密闭真空恒容容器中(固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s)  2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是?
2NH3(g)+CO2(g)。判断该分解反应已经达到化学平衡的是?
A.2v(NH3)=v(CO2)
B.密闭容器中c(NH3)∶c(CO2)=2∶1
C.密闭容器中混合气体的密度不变
D.密闭容器中氨气的体积分数不变
参考答案:C
本题解析:该反应为有固体参与的非等体反应,且容器体积不变,所以压强、密度均可作标志,该题应特别注意D项,因为该反应为固体的分解反应,所以NH3、CO2的体积分数始终为定值(NH3为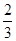 ,CO2为
,CO2为 )。
)。
本题难度:一般
4、选择题 哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1molN2和3molH2,在一定条件下发生反应N2+3H2 2NH3?。下列有关说法正确的是:
2NH3?。下列有关说法正确的是:
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
C.达到化学平衡时,反应则停止进行
D.当反应达到平衡时,每有3mol的H―H断裂,同时就有6mol的N―H键断裂。
参考答案:BD
本题解析:A.N2+3H2 2NH3反应是可逆反应,反应物可转化为生成物,生成物也可转化为反应物,所以反应物不能完全转化为生成物。错误。B.由于该反应是在体积恒定的密闭容器中发生的反应前后气体体积不等的反应。当反应达到化学平衡时,反应混合物中的任何成分N2、H2和NH3的物质的量浓度不再变化。正确。C.当反应达到化学平衡时,反应物还在反应产生生成物,生成物还在反应变为反应物,只是单位时间内任何物质消耗的浓度与产生的浓度相等,因此反应并未停止,任然在进行。错误。D.在任何时刻若有3mol的H―H断裂,就会有6mol的N―H键形成,同时有6mol的N―H键断裂。则相同的时间内N―H键形成与断裂数目相等,氨气的浓度不变,则反应达到平衡。正确。
2NH3反应是可逆反应,反应物可转化为生成物,生成物也可转化为反应物,所以反应物不能完全转化为生成物。错误。B.由于该反应是在体积恒定的密闭容器中发生的反应前后气体体积不等的反应。当反应达到化学平衡时,反应混合物中的任何成分N2、H2和NH3的物质的量浓度不再变化。正确。C.当反应达到化学平衡时,反应物还在反应产生生成物,生成物还在反应变为反应物,只是单位时间内任何物质消耗的浓度与产生的浓度相等,因此反应并未停止,任然在进行。错误。D.在任何时刻若有3mol的H―H断裂,就会有6mol的N―H键形成,同时有6mol的N―H键断裂。则相同的时间内N―H键形成与断裂数目相等,氨气的浓度不变,则反应达到平衡。正确。
本题难度:一般
5、选择题 反应A(g)+3B(g) 2C(g)+2D(g),在不同条件下测得反应速率,其中速率最快的是
2C(g)+2D(g),在不同条件下测得反应速率,其中速率最快的是
[? ]
A.?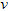 (D)=0.4?mol?/(L・s)
(D)=0.4?mol?/(L・s)
B.?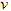 (C)=0.5?mol?/(L・s)
(C)=0.5?mol?/(L・s)
C.?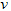 (B)=0.6?mol?/(L・s)
(B)=0.6?mol?/(L・s)
D.?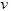 (A)=0.15?mol?/(L・s)
(A)=0.15?mol?/(L・s)
参考答案:B
本题解析:
本题难度:简单