1������� ��14�֣�ʵ�������������������������з�����ȡ�ģ�
4HCl��Ũ����MnO2 Cl2����MnCl2��2H2O
Cl2����MnCl2��2H2O
�Իش��������⣺
��1���÷�Ӧ��������ԭ��Ӧ��?�������������ԭ��Ӧ����ָ��___?����������?�ǻ�ԭ����_________���������________�ǻ�ԭ�����������������ԭ��Ӧʽ�ж������ԣ�______��_______����ԭ�ԣ�______��_______��
��д���÷�Ӧ�����ӷ���ʽ?_________?
����˫���ŷ�����÷�Ӧ����ת�Ƶķ������Ŀ? _______________________________
�ο��𰸣�. ��?��? MnO2? HCl? Cl2? MnCl2?MnO2��Cl2? HCl��MnCl2
��2��4H++2Cl-+MnO2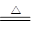 Cl2��+Mn2++2H2O
Cl2��+Mn2++2H2O
(3) 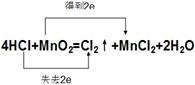
�����������1�����ݷ�Ӧ�ķ���ʽ��֪����Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ�����Ԫ�صĻ��ϼ۴ӣ�4�۽��͵���2�ۣ���������������ԭ��Ӧ�������������Ƕ������̣�HCl�ǻ�ԭ��������������������Ȼ�þ�ǻ�ԭ���������������ԭ��Ӧ����������������ǿ����������ģ���ԭ���Ļ�ԭ��ǿ�ڻ�ԭ����ģ����������Ժͻ�ԭ��ǿ��˳��ֱ���MnO2��Cl2��HCl��MnCl2��
��2���Ȼ�����Ȼ��̶��ǿ��Բģ����Ը÷�Ӧ�����ӷ���ʽ��
4H++2Cl-+MnO2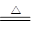 Cl2��+Mn2++2H2O��
Cl2��+Mn2++2H2O��
��3��˫�����������յ��Ԫ����ͬһ�֣����Ը�������ԭ��Ӧ�ı�ʾ��
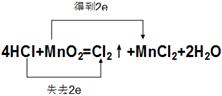
�������ڽ���������ԭ��Ӧ���й��ж�ʱ���ؼ�ʱȷ����й�Ԫ�صĻ��ϼ۱仯�����Ȼ�������йصĸ�����з����жϼ��ɡ�
�����Ѷȣ�һ��
2��ѡ���� ���з�Ӧ����ʽ����һ�������������ڷ����ϲ�ͬ�������Ӧ��
A��2Mg + O2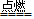 2MgO
2MgO
B��Zn +2HCl �� ZnCl2 + H2��
C��NaCl + AgNO3�� AgCl��+ NaNO3
D��CuO + H2 Cu + H2O
Cu + H2O
�ο��𰸣�C
�����������ȷѡ��ΪC���÷�ӦΪ���ֽⷴӦ���ڷ�������ԭ��Ӧ����������ѡ��Ϊ������ԭ��Ӧ��
�����Ѷȣ�һ��
3��ѡ���� ������������ȷ����(����)
A���е������ɵķ�Ӧһ����������ԭ��Ӧ
B���ǽ�������ۺ����ᶼ����ǿ������
C�����ֲ�ͬ������������Һ��һ���ܴ�������
D��ͬ�������е�ͬ��Ԫ���ڷ�Ӧ�п��ܼȱ������ֱ���ԭ
�ο��𰸣�D
���������A����ȷ�������������ɳ����ȣ�B����ȷ������̼��ȣ�C����ȷ������OH����HCO3���ȣ������ȷ�Ĵ�ѡD��
�����Ѷȣ�һ��
4������� (12��)��֪��Ӧ����SO3��H2O===H2SO4����3NO2��H2O===2HNO3��NO
��2F2��2H2O===4HF��O2����2Na��2H2O===2NaOH��H2����
��Na2O��2HCl===2NaCl��H2O����SiO2��2NaOH===Na2SiO3��H2O
(1)������Ӧ�в�����������ԭ��Ӧ����______________________ (����ţ���ͬ)��
H2O����������______��H2O����ԭ����______������������ԭ��Ӧ�������е�H2O�Ȳ��������ֲ�����ԭ����__________________��
(2) ��˫���ŷ�����Ӧ�ڣ�______________________________________________.
(3) �õ����ű����Ӧ�۵ĵ���ת�Ʒ������Ŀ_________________________.
(4)д����Ӧ�ܵ����ӷ���ʽ��______________________________________________.
�ο��𰸣�(12��)
(1)�٢ݢ� (����ţ���ͬ)�� �ۡ�? �ܡ�? �ڣ�
��2��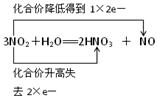
 ��3��
��3��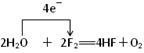
(4)? 2Na��2H2O===2Na��+2OH����H2��
�����������1�����ݷ���ʽ��֪���٢ݢ���Ԫ�صĻ��ϼ۶�û�б仯������������ԭ��Ӧ�����ڷ�Ӧ���У���Ԫ�صĻ��ϼ۲������ߵ���5�ۣ����ֽ��͵���2�ۣ����NO2������������Ҳ�ǻ�ԭ������ˮ�Ȳ�����������Ҳ���ǻ�ԭ������Ӧ��FԪ�صĻ��ϼ۴�0�۽��͵���1�ۣ����ʷ�������������ˮ����Ԫ�صĻ��ϼ۴ӣ�2�����ߵ�0�ۣ�ʧȥ���ӣ�����ԭ������Ӧ���У���Ԫ�صĻ��ϼ۴�0�����ߵ���1�ۣ�ʧȥ���ӡ�ˮ����Ԫ�صĻ��ϼ۴ӣ�1�۽��͵�0�ۣ�����õ����ӣ�����������
��2��˫���ŷ�����ʾͬ��Ԫ�ص�ԭ���ڷ�Ӧǰ��ת�Ƶ��ӵ��������ͷ�ӷ�Ӧ��ָ������������ʾ����ת�Ƶķ�������������ͬ��Ԫ�أ����Ӧ�ñ�ʾΪ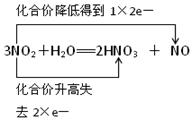 ��
��
��3���������м�ͷ�ӻ�ԭ����ʧ���ӵ�Ԫ��ָ���������õ��ӵ�Ԫ�أ����ڼ�ͷ�ķ����Ѿ�ָ������ת�Ƶķ������Բ���Ҫע����ʧ��������ע������ת�Ƶ���Ŀ����Ӧ�ñ�ʾΪ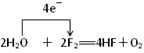 ��
��
��4�����ݻ�ѧ����ʽ��֪���÷�Ӧ�����ӷ���ʽ��2Na��2H2O===2Na��+2OH����H2����
������������Ԫ�ػ��ϼ������ķ�Ӧ����������ԭ��Ӧ��û��Ԫ�ػ��ϼ������ķ�Ӧ�Ƿ�������ԭ��Ӧ�������ж�������ԭ��Ӧ�Ĺؼ���ȷ�ж�Ԫ�صĻ��ϼ۱仯��
�����Ѷȣ�һ��
5��ѡ���� ijϡ��Һ�к��е����ʵ�����(��Ϊ1mol)ZnSO4��Fe2(SO4)3��H2SO4��CuSO4���������������ۡ����и�ͼ��ʾ��Һ�е�Fe2+�����ʵ�����������۵����ʵ���֮��Ĺ�ϵ��������ȷ����(? )
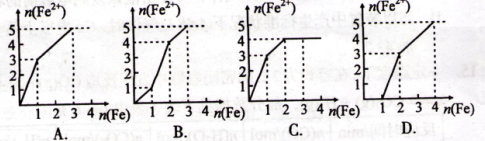 ?
?
�ο��𰸣�A
����������������ۺ��������ӷ�Ӧ��˳��Ϊ��Fe+2Fe3+= 3Fe2+��n(Fe)��n(Fe2+)=1��3���ٷ�����Ӧ��Fe+Cu2+=Cu+Fe2+��Fe+2H+=Fe2+ +H2���� n(Fe)��n(Fe2+)=l��1�����Դ�A��ȷ��
�����Ѷȣ�һ��