1、实验题 甲同学拟通过实验探究同主族元素性质的递变规律,以及影响化学反应速率的因素。其设计的实验方案如下,请你帮他填写完整,并做出评价。实验室提供的试剂:锌块、锌粉、铁条、铁粉、铜条、NaBr溶液、NaI溶液、新制的氯水、1mol/?盐酸、3mol/L的盐酸
(1)探究同主族元素性质的递变规律
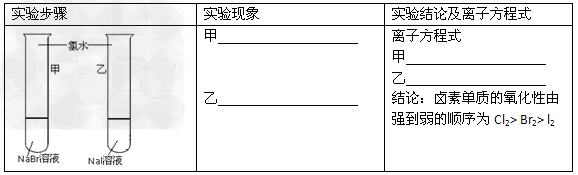
【评价】甲同学设计的实验方案的合理性是___________(填序号)
A.?非常合理 B.?部分合理 C.?完全不合理
【补充和完善】上一项若填A,则此项不用再作答,若填B或C,则完成实验还需要的试剂是___________。
(2)探究影响化学反应速率的因素

甲同学所得实验依据和结论有明显问题,问题是__________。
(3)请你利用原电池原理,设计实验,比较铜和铁的金属活动性。画出实验装置图,标出正负极、电子流动方向,写出电极反应式。
①
②电极反应式 ____________________________、____________________________
2、选择题 下列不同条件下的化学反应A+B=C+D,反应速率按由大到小的顺序排列,正确的一组是
[? ]
①常温下20 mL含A和B各0.001 mol
②常温下100 mL含A和B各0.01 mol
③常温下0.05 mol/L的A,B溶液各10 mL,再加入蒸馏水20 mL
④常温下100 mL含A 0.01 mol和20 mL 含B 0.001 mol
A.①②③④
B.④③②①
C.②④①③
D.②①④③
3、选择题 化学中常用图象直观地描述化学反应的进程或结果,下列图象描述正确的是( )

A.图①可以表示对某化学平衡体系改变温度后反应速率随时间的变化
B.图②表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(g)的影响,且乙的压强大
C.图③表示向Al2(SO4)3和MgSO4的混合液中滴加NaOH溶液,生成沉淀的量与滴入NaOH溶液体积的关系
D.根据图④可确定除去CuSO4溶液中的Fe3+可以向溶液中加入Cu(OH)2调节pH至4左右
4、填空题 某温度下,在密闭容器中SO2、O2、SO3三种气态物质建立化学平衡后,改变条件对反应2SO2(g)+O2(g)  2SO3(g),ΔH < 0的正、逆反应速率的影响如图所示:
2SO3(g),ΔH < 0的正、逆反应速率的影响如图所示:

(1)加催化剂对反应速率影响的图像是________(填序号,下同),平衡________移动。
(2)升高温度对反应速率影响的图像是________,平衡向________方向移动。
(3)增大反应容器体积对反应速率影响的图像是________,平衡向________方向移动。
(4)增大O2的浓度对反应速率影响的图像是__________,平衡向________方向移动。
5、选择题 下列关于化学反应速率的说法正确的是
A.对任何化学反应来说,反应速率越大,反应现象就越明显
B.化学平衡指化学反应的最大限度,改变条件也不能改变化学平衡
C.可逆反应达到化学平衡状态时,正、逆反应的速率都为0
D.升高温度一定能增大反应速率