1������� ��ŨHNO3�з���ͭƬ:��16�֣�
��1����Ӧ��ʼʱ�Ļ�ѧ����Ϊ?��
��2������ͭʣ�࣬��Ӧ��Ҫ����ʱ�Ļ�ѧ����ʽΪ?��
��3������Ӧֹͣʱ���ټ�������25%��ϡ���ᣬ��ʱͭƬ���������ݲ�������ԭ������ӷ���ʽ��?��
��4������12.8gͭ��һ��������Ũ���ᷴӦ��ͭ����ʱ������������5.6 L(��״��������������������ʵ�����?�����������ƽ����Է�������Ϊ?��
��5��������4���������������100mL ��Һ�����в�������ʹ������ҺŨ��ƫС����_______ ___����д��ţ���
��δϴ���ձ��Ͳ������ڶ���ҡ�Ⱦ��ú���Һ����ڿ̶��ߺ������ˮ����Һ����̶������Т�����Һǰ����ƿ������������ˮ�ܶ���ʱ��������ƿ�Ŀ̶���
��������ͭ�����ʵ���Ũ��Ϊ?mol/L��
�ο��𰸣���16�֣���1��Cu + 4 HNO3��Ũ��="==" Cu(NO3)2 + 2 NO2��+2 H2O
(2) 3 Cu + 8 HNO3��ϡ��="==" 3Cu(NO3)2 + 2 NO��+4 H2O
��3������ϡ�����ṩ��H +�� NO3���������������ֿ���Cu��Ӧ
3 Cu + 8 H + + 2 NO3�� ="=" 3 Cu2+ + 2 NO��+4 H2O
��4��0.65mol? 41.2
��5���٢�? 2mol/L
���������
��1��Cu + 4 HNO3��Ũ��="==" Cu(NO3)2 + 2 NO2��+2 H2O
(2) ��Ӧһ��ʱ��������ϡ��3 Cu + 8 HNO3��ϡ��="==" 3Cu(NO3)2 + 2 NO��+4 H2O
��3��Cu(NO3)2�е�NO3�D,����ϡ�����ṩ��H +�� NO3���������������ֿ���Cu��Ӧ
3 Cu + 8 H + + 2 NO3�� ="=" 3 Cu2+ + 2 NO��+4 H2O
��4�������ɵ�NO��NO2�����ʵ����ֱ���x��y
x+y=5.6/22.4
�ɵ����غ�ã�2��12.8/64=3x+y
���x=0.075mol? y=0.175mol?
n(HNO3)=2n(Cu?)��n(NO)��n(NO2)=0.075mol��0.175mol��2��12.8/64mol=0.65mol
��������ƽ����Է�������Ϊ����0.075��28��0.175��46��/0.25=41.2
��5���٢�ƫ�ͣ��۲���Ӱ���ƫ��
c(Cu (NO3)2)=0.2mol/0.1L=2mol/L
�����Ѷȣ�һ��
2��ѡ���� ͬ����Ԫ���γɵ�ͬһ����������ڽṹ�������Ϻ����ơ�������PH4I��һ�ְ�ɫ���壬���ж�PH4I����������ȷ���ǣ�?��
A������һ�ֹ��ۻ�����
B������ʱPH4I���Էֽ⣬��������ɫ�仯
C�������Ը�NaOH��Ӧ
D��������PH3��HI���϶���
�ο��𰸣�B
���������PH4I�ֽ�����PH3��HI��HI�ڼ��������»�ֽ�����H2������ɫ��I2��ע�⣺NH4Cl�ֽ�����NH3��HCl��HCl�����ֽ⣩�����B����ȷ�ġ�
�����Ѷȣ���
3��ѡ���� �������ʶ����н�ǿ����ˮ�ԡ���ʹϡ�����ΪŨ���ᣬ����ʹ�õ��Լ���
A��Ũ����
B������������
C����ˮ����þ
D������
�ο��𰸣�D
���������A��Ũ���������ˮ�ԣ���ʹϡ�����ΪŨ���ᣬA��ȷ��B��������������ѧ��ˮ��Ϊ���ᣬ������ʹϡ�����ΪŨ���ᣬB��ȷ��C����ˮ����þ������ˮ�ԣ���ʹϡ�����ΪŨ���ᣬC��ȷ��D�������DZ�������ˮ���ܣ�����ʹϡ�����ΪŨ���ᣬD����ȷ����ѡD��
�����Ѷȣ���
4��ѡ���� �ɷ�Ӧ8NH3+3Cl2====N2+6NH4Cl��֪��30 mL Cl2��������ͬ�����µ�NH3�����Ϊ��?��
A��80 ml
B��40 mL
C��20 mL
D��10 mL
�ο��𰸣�C
���������������NH3ռ����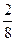 ��
��
�����Ѷȣ���
5������� ������һ���ḻ���ʱ��⣬ͨ����ˮ���ۺ����ÿɻ���������ʹ�����ʹ�á�
��1����ˮ���εĿ������ã�
�ٺ�ˮ����Ŀǰ�����Ϊ�������������ѡ��Զ�뽭���뺣�ڣ�������꣬��ϫ��������ƽ̹�տ��ĺ�̲�����������Ϊ��ˮ�ء������غ�?�ء�
��Ŀǰ��ҵ�ϲ��ñȽ��Ƚ������ӽ���Ĥ���۷������ȼҵ�������ڵ����������ӽ���Ĥֻ����������ͨ������ֹ�����Ӻ�����ͨ������˵���ȼ������������ӽ���Ĥ�����ã�?��дһ�㼴�ɣ���
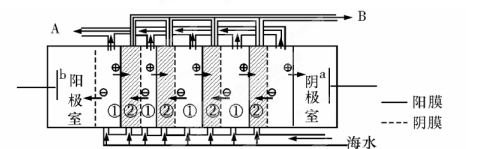
��2�����������ǽ��귢չ���һ�ֽϺõĺ�ˮ������������ԭ����ͼ��ʾ�����о���ѡ���Ե������ӽ���Ĥ�������ӽ���Ĥ������С���ش���������⣺
�ٺ�ˮ����ֱ��ͨ�뵽�������У�������?��
��A���ų�����?�����ˮ����Ũˮ������
��3���ÿ�±���� �����ӣ�����ȡ�壬�������������£�
�����ӣ�����ȡ�壬�������������£�
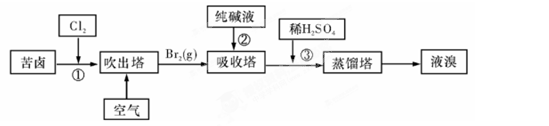
�����������е���Һ��BrO3-�����������з�Ӧ�����ӷ���ʽΪ��?��
��ͨ�����Ȼ��ѻ�ú�Br2����Һ��Ϊ�λ��辭�����������ա��ữ���»�ú�Br2����Һ��?��
������������ͨ��ˮ�������ȣ������¶���90�����ҽ��������ԭ����?��
�ο��𰸣���1���ٽᾧ?����ֹH2��Cl2������Ӧ����������ը����ֹCl2�����ɵ�NaOH��Һ��Ӧ��ʹ�ռ��Ʒ�����ȣ�����������Ҳ���֣�
��2���ٺ�ˮ�к��϶�Mg2+��Ca2+�������ӣ����ʱ�����Mg��OH��2��Ca��OH��2�ȳ����Ӷ����������ӽ���Ĥ������������Ҳ���֣���3�֣��ڵ�ˮ
��3����3CO32-+3Br2=5Br-+BrO3-+3CO2��
�ڸ����壬���Br2��Ũ�ȣ�����������Ҳ���֣�
���¶ȹ������Խ�Br2������������¶ȹ����ֻὫ������ˮ�������
�����������1���ٺ�ˮ������Ҫ�������������ᾧԭ���������������Ϊ��ˮ�ء������غͽᾧ�ء����ȼ����������������ڻ�����������������������ӽ���Ĥ�����ã���ֹH2��Cl2������Ӧ����������ը����ֹCl2�����ɵ�NaOH��Һ��Ӧ��ʹ�ռ��Ʒ�����ȡ�
��2���ٺ�ˮ�к��϶�Mg2+��Ca2+�������ӣ����ʱ�����Mg��OH��2��Ca��OH��2�ȳ����Ӷ����������ӽ���Ĥ���ʺ�ˮ����ֱ��ͨ�뵽�������С���A���ų����ǵ�ˮ��
��3�����ÿ�±��ȡ�壬�������з����ķ�ӦΪ����̼���Ƶķ�Ӧ���������к�BrO3-����Ӧ����ʽΪ3CO32-+3Br2=5Br-+BrO3-+3CO2������ͨ�����Ȼ��ѻ�ú�Br2����Һ�������Ũ��̫�ͣ��������ռ����������������ա��ữ���»�ú�Br2����Һ��Ϊ�˸����壬���Br2��Ũ�ȣ����¶ȹ������Խ�Br2������������¶ȹ����ֻὫ������ˮ���������������������ͨ��ˮ�������ȣ������¶���90�����ҽ�������
�����Ѷȣ�һ��