1、实验题
为了探究草酸(H2C2O4)的化学性质,设计如下3个实验:
实验1:取一定量草酸溶液装入试管,加入一定体积的酸性高锰酸钾溶液,振荡试管,发现溶液开始缓慢褪色,后来迅速变成无色。(反应热效应不明显,可忽略不计)
(1)该实验说明草酸具有________(填“氧化”或“还原”)性,该反应的反应速率先慢后快的主要原因可能是__________________。
实验2:取少量草酸晶体装入试管,加水溶解,向试管里滴加足量的澄清石灰水,有白色沉淀生成。
(2)该实验说明草酸具有______性。写出反应的化学方程式:__________________。
实验3:草酸在常温下呈无色晶体状,其晶体的熔化温度低于草酸的分解温度,且易升华。为了探究草酸的不稳定性,某同学设计如下实验装置
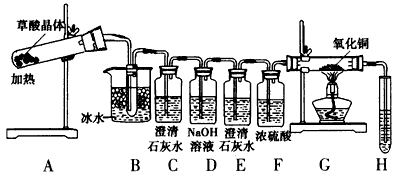
(3)B装置的作用是__________________。C装置变浑浊,E处无现象,G玻璃管里黑色变红色,写出A中反应的化学方程式:__________________。
(4)为了检验G中反应的氧化产物,H试管所装试剂是___________,从环境保护角度来看,该方案的不足之处是________________________。
参考答案:
(1)还原;锰离子起催化作用或锰离子浓度增加,加快了反应速率
(2)酸;Ca(OH)2+H2C2O4=CaC2O4↓+2H2O
(3)冷凝草酸蒸气,避免对二氧化碳的检验产生干扰;H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
(4)澄清石灰水(或偏铝酸钠溶液或硅酸钠溶液等);没有尾气处理装置
本题解析:
本题难度:一般
2、填空题 金属钠与水的反应是中学化学中的一个重要反应.在高中化学教材的几次改版中该实验曾出现过几种不同的演示方法,分别如图中甲、乙、丙所示:
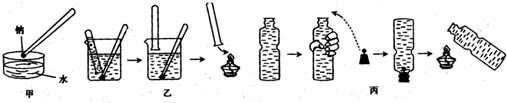
(1)现按图甲所示的方法,在室温时,向盛有Ca(HCO3)2溶液的水槽中,加入一小块金属钠.下列现象描述正确的是______(填字母).
A.钠浮在液面上,并四处游动,最后消失?B.钠熔化成一个光亮的小球
C.反应开始后,溶液由无色变红色? D.恢复到室温时,烧杯底部有固体物质析出
(2)请补充并完成甲实验中从试剂瓶中取出钠到向水槽中投入钠的有关操作:用镊子从试剂瓶中取出一小块钠→______→用镊子夹取切好的金属钠投入到盛有Ca(HCO3)2溶液的烧杯中.
(3)按图乙所示方法来收集产生的气体,需将钠包好,再放入水中.取相同质量的钠按下列几种情况收集产生的气体在相同条件下体积最大的是______
A.用铝箔包住钠?B.用锡箔包住钠?C.直接将钠投入的水中
(4)用装满水的矿泉水瓶按图丙方法进行实验,用手挤压矿泉水瓶并塞紧带有钠的塞子,共排出水的体积为16.8mL,待钠反应结束后,干瘪的带塞矿泉水瓶恢复成原状,假设瓶内、瓶外均属于标准状况,则所用的钠的质量为______g.
参考答案:(1)将钠投入到碳酸氢钙溶液中,钠先和水反应,呈现的现象是:钠浮在水面上,熔化成一个光亮的小球,并四处游动,最后消失,生成的氢氧化钠和碳酸氢钙反应生成难溶性的碳酸钙,所以恢复到室温时,烧杯底部有固体物质析出,故选ABD;
(2)做钠和水的反应实验时,用滤纸吸干表面的煤油,在玻璃生上用小刀切成绿豆大小的钠粒,并将多余的钠放回试剂瓶中,故答案为:用滤纸吸干表面的煤油,在玻璃生上用小刀切成绿豆大小的钠粒,并将多余的钠放回试剂瓶中;
(3)钠和水反应生成氢气和氢氧化钠,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,锡和氢氧化钠溶液不反应,所以生成氢气体积最大的是用铝箔包住钠,故选A;
(4)该反应中排出水的体积就是氢气的体积,设消耗的钠的质量是x,
2Na+2H2O=H2↑+2NaOH
46g? 22.4L
x? 0.0168L
x=0.0168L×46g22.4L=0.0345g,
故答案为:0.0345.
本题解析:
本题难度:一般
3、选择题 下列物质的鉴别方法不正确的是( )
A.用焰色反应鉴别NaCl溶液和Na2SO4溶液
B.用品红试液鉴别SO2和CO2两种气体
C.用盐酸溶液鉴别Na2CO3溶液和Na2SiO3溶液
D.利用丁达尔效应鉴别淀粉胶体和NaOH溶液
参考答案:A、焰色反应是金属元素的性质,硫酸钠和氯化钠中都有钠元素,焰色反应相同,所以不能用焰色反应鉴别,可以用氯化钡鉴别,故A错误;
B、二氧化硫有漂白性,能使品红溶液褪色,二氧化碳没有漂白性不能使品红溶液褪色,所以可以用品红鉴别二氧化碳和二氧化硫,注意不能用澄清石灰水鉴别二氧化硫和二氧化碳,因为它们都能使澄清石灰水变浑浊,故B正确;
C、盐酸和碳酸钠反应生成二氧化碳气体,和硅酸钠反应生成不溶性的硅酸,反应现象不同,所以可以用盐酸鉴别碳酸钠和硅酸钠,故C正确;
D、淀粉胶体能产生丁达尔效应,氢氧化钠溶液不能产生丁达尔效应,反应现象不同,所以可以用丁达尔效应检验氢氧化钠溶液和淀粉胶体,故D正确.
故选A.
本题解析:
本题难度:简单
4、实验题 (6分)某实验小组用下列装置进行乙醇催化氧化的实验。已知:乙醛可被氧化为乙酸。
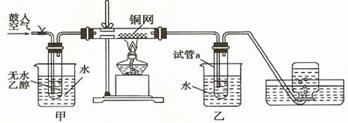
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式___________________。
⑵在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应
是?反应。
⑶若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有?。要除去该物质,可在混合液中加入?(填写字母)。
A.氯化钠溶液
B.苯
C.碳酸氢钠溶液
D.四氯化碳