| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点大全《电解池原理》试题预测(2020年最新版)(八)
参考答案:C 本题解析:从电解的方程式看出Al在阳极放电,Al接电源的正极,Cu接电源的负极,H+在阴极放电。Cu接电源的负极,A错;聚合氯化铝不带电,根据化合价代数和为零,3×2-1×m-(x-m)=0,得x=6,B错;电解时阴极是阳离子放电,是H+在阴极放电生成H2,C对;将电源换成导线连接两电极,满足原电池的形成条件,可以形成原电池,D错。 本题难度:困难 2、选择题 用惰性电极电解下列溶液,一段时间后,再加入一定质量的另一物质中(括号内),溶液能与原来溶液完全一样的是 |
参考答案:C
本题解析:A.惰性电极电解氯化铜溶液,电极生成物是氯气、铜,所以需要加入的是氯化铜,A错误;B.惰性电极电解氢氧化钠溶液,实质是电解水,加入的应该是水,B错误;C.电解氯化钠溶液生成氢气、氯气和氢氧化钠溶液,需要加入的是HCl,C正确;D.惰性电极电解硫酸铜溶液,生成物是铜、氧气和硫酸,所以需要加入的是氧化铜或碳酸铜,加入氢氧化铜会相当于多加水,D错误;答案选C。
考点:考查电解原理。
本题难度:一般
3、选择题 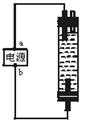
A.a为正极,b为负极;NaClO和NaCl
B.a为负极,b为正极;NaClO和NaCl
C.a为阳极,b为阴极;HClO和NaCl
D.a为阴极,b为阳极;HClO和NaCl
参考答案:B
本题解析:用石墨作电极电解饱和氯化钠溶液发生的反应是:2NaCl+2H2O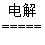 2NaOH+H2↑+Cl2↑,伴随电解过程所发生的副反应是2NaOH+Cl2===NaCl+NaClO+H2O,则可推知使Cl2被完全吸收制得有较强杀菌能力的消毒液主要成分是NaClO和NaCl溶液,起消毒作用的是NaClO溶液。电解过程阴极产生氢气,结合图示,消毒液发生器的液体上部空间充满的是氢气,从中推知电源a极是负极,b为正极。所以B选项符合题意。
2NaOH+H2↑+Cl2↑,伴随电解过程所发生的副反应是2NaOH+Cl2===NaCl+NaClO+H2O,则可推知使Cl2被完全吸收制得有较强杀菌能力的消毒液主要成分是NaClO和NaCl溶液,起消毒作用的是NaClO溶液。电解过程阴极产生氢气,结合图示,消毒液发生器的液体上部空间充满的是氢气,从中推知电源a极是负极,b为正极。所以B选项符合题意。
本题难度:简单
4、填空题 (1)?电池反应通常是放热反应,下列反应在理论上可设计成原电池的化学反应是____________?(填序号)。此类反应具备的条件是①__________反应,②_________反应。 ?
A.C(s)+H2O(g)==CO(g)+H2(g):△H>0?
B.Ba(OH)2・8H2O(s)+2NH4Cl(s)==BaCl2(aq)+2NH3・H2O( ?)+8H2O(
?)+8H2O(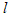 ?)△H>0 ?
?)△H>0 ?
C.CaC2(s)+2?H2O( )==Ca(OH)2(s)+C2H2(g);△H<0 ?
)==Ca(OH)2(s)+C2H2(g);△H<0 ?
D.CH4(g)+2O2(g)==CO2(g)+2H2O(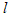 ?):△H<0
?):△H<0
(2)?以KOH溶液为电解质溶液,依据(I)所选反应设计一个电池。其负极反应为:________。
(3)?电解原理在化学工业中有广泛的应用。现将你设计的原电池通过导线与图中电解池相连,其中a为电解液,X和Y是两块电极扳,则 ?
①若X和Y均为惰性电极,a为饱和食盐水,则电解时检验Y电极反应产物的方法是______?。?
②若X、Y分别为石墨和铁,a仍为饱和的NaCI溶液,则电解过程中生成的白色固体露置在空气中,可观察到的现象是____________。 ?
③若X和Y均为惰性电极,a为一定浓度的硫酸铜溶液,通电后,发生的总反应化学方程式为___________。通电一段时间后,向所得溶液中加入0.05?mol?Cu(OH)2,恰好恢复电解前的浓度和PH,则电解过程中电子转移的物质的量为______________mol。
(4)利用工业上离子交换膜法制烧碱的原理,用如下图所示装置电解K2SO4溶液。
①?该电解槽的阳极反应式为___________,通过阴离子交换膜的离子数___________(填“>”、“<”或“=”)通过阳离子交换膜的离子数;
②?图中a、b、c、d分别表示有关溶液的pH,则a、b、c、d由小到大的顺序为___________?;
③?电解一段时间后,B口与C口产生气体的质量比为__________。 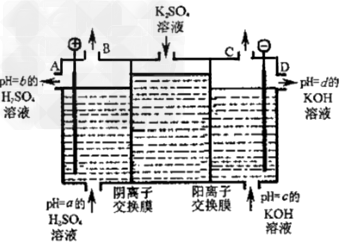
参考答案:(1)D、放热、氧化还原
(2)CH4-8e-+10OH-=C?+7H2O?
(3)①将湿润的淀粉碘化钾试纸靠近Y极支管口,试纸变蓝。
? ②白色固体迅速变灰绿色,最终变成红褐色。?
? ③?;0.2
(4)①4OH--4e-=2H2O+O2?↑ ;?<;?②?b<a<c<d ; ③ 8:1
本题解析:
本题难度:一般
5、选择题 用铂电极电解下列溶液时,阴极和阳极上的主要产物分别为H2和O2的是
[? ]
A、稀NaOH溶液?
B、HCl溶液?
C、CuSO4溶液?
D、酸性AgNO3溶液
参考答案:A
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《盖斯定律》.. | |