1、选择题 下列说法中正确的是
A.铁的摩尔质量就是铁的相对原子质量
B.CO32-的摩尔质量是60g/mol
C.1molO2的质量是32g/mol
D.CO2的摩尔质量是44g
参考答案:B
本题解析:A、摩尔质量以g/mol为单位,数值上等于相对原子质量;
C、质量单位为g,D、摩尔质量单位为g/mol。
本题难度:困难
2、填空题 (7分)已知:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,用双线桥法标出上述电子转移的方向和数目:__ _。上述反应中还原剂是________;氧化剂是_______。
参考答案: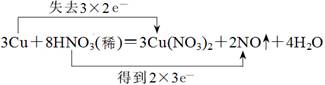 还原剂Cu(2分)氧化剂HNO3(2分)
还原剂Cu(2分)氧化剂HNO3(2分)
本题解析:在该反应中,Cu元素的化合价升高为+2价,N元素的化合价由+5价降到+2价,所以方程式中Cu共失去6个电子,N元素共得到6个电子,用双线桥表示为 ,失去电子的物质发生氧化反应,本身做还原剂,所以Cu是还原剂;得到电子的物质,发生还原反应,本身做养护剂,所以硝酸是氧化剂。
,失去电子的物质发生氧化反应,本身做还原剂,所以Cu是还原剂;得到电子的物质,发生还原反应,本身做养护剂,所以硝酸是氧化剂。
考点:考查氧化还原反应的分析
本题难度:一般
3、选择题 已知,同温度下的溶解度:Zn(OH)2>ZnS,MgCO3>Mg(OH)2;就溶解或电离出S2-的能力而言,FeS?>H2S?>CuS,则以下离子方程式错误的是
A.Mg2+ + 2 HCO3- + 2Ca2+ + 4 OH- → Mg(OH)2↓ + 2CaCO3↓ + 2H2O
B.Cu2+ + H2S → CuS↓ + 2H+
C.Zn2+ + S2- + 2H2O → Zn(OH)2↓ + H2S↑
D.FeS + 2H+ →Fe2+ + H2S↑
参考答案:C
本题解析:
本题难度:简单
4、选择题 木炭与浓硫酸反应可表示为:C +2H2SO4(浓)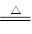 CO2↑+2SO2↑+2H2O。
CO2↑+2SO2↑+2H2O。
(1)该反应的反应物和生成物中,属于氧化物的是 。
(2)木炭作 (填“氧化剂”或“还原剂”),硫酸 (填“被氧化”或“被还原”)。
(3)若消耗了2mol H2SO4,则生成 mol SO2。
参考答案:(1)CO2 、SO2、 H2O (2)还原剂 被还原 (3)1
本题解析:氧化物是由氧和另一种元素组成的化合物,即氧化物的组成元素有两种,其中一种为氧元素。根据氧化物的定义可知该反应的反应物和生成物中,属于氧化物的是CO2 、SO2、H2O。(2)在反应中C的化合价由反应前单质中的0价变为反应后CO2中的+4价,化合价升高,失去电子,被氧化,作还原剂;H2SO4中的S的化合价一部分由反应前的+6价变为反应后SO2中的+4价,化合价降低,得到电子,被还原,作氧化剂,还有一部分未参加氧化还原反应,起酸的作用,提供酸根离子用来结合形成盐。每有2摩尔的浓H2SO4参加反应,产生1摩尔的SO2。
考点:考查木炭与浓硫酸反应中的电子转移、氧化剂、还原剂及反应类型等的判断的知识。
本题难度:一般
5、选择题 下列溶液中,Na+ 物质的量浓度最大的是
A.1mL 0.5mol・L-1的NaAlO2溶液
B.100mL 0.01 mol・L-1的NaCl溶液
C.10mL 0.1mol・L-1的NaOH溶液
D.100mL 0.1mol・L-1的Na2SO3溶液
参考答案:A
本题解析:试题分析:ABCD 中钠离子的浓度分别是:0.5mol・L-1?,0.01mol・L-1?,0.1mol・L-1,0.2mol・L-1,所以浓度最大的是A ,故选A 。
考点:物质的量浓度
点评:解答本题学生需要注意的是:对于给定的溶液,浓度和体积没关系,浓度是标量。
本题难度:一般