1、选择题 相同条件下能进行以下三个反应:①2A-+B2═A2+2B-;②2C-+A2═2A-+C2;③2B-+D2═2D-+B2.由此可得出的分析结论正确的是( )
A.氧化性:A2>B2>C2>D2
B.还原性:C-<A-<B-<D-
C.2A-+D2═2D-+A2的反应可以发生
D.2B-+C2═2C-+B2的反应可以发生
参考答案:A、氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,在反应2A-+B2═A2+2B-中,氧化剂是B2,氧化产物是A2,所以氧化性B2>A2,在反应2C-+A2═2A-+C2中,氧化剂是A2,氧化产物是C2,所以氧化性A2>C2,在反应2B-+D2═2D-+B2中,氧化剂是D2,氧化产物是B2,所以氧化性D2>B2,综上氧化性顺序是:D2>B2>A2>C2,故A错误;
B、氧化还原反应中,还原剂的还原性大于还原产物的还原性,在反应2A-+B2═A2+2B-中,还原剂是A-,还原产物是B-,所以还原性A->B-,在反应2C-+A2═2A-+C2中,还原剂是C-,还原产物是A-,所以还原性C->A-,在反应2B-+D2═2D-+B2中,还原剂是B-,还原产物是D-,所以还原性B->D-,综上还原性顺序是:C->A->B->D-,故B错误;
C、氧化性顺序是:D2>B2>A2>C2,即D2的氧化性强于A2,则反应2A-+D2═2D-+A2可以发生,故C正确;
D、氧化性顺序是:D2>B2>A2>C2,所以C2的氧化性弱于B2,则反应2B-+C2═2C-+B2不可能发生,故D错误;
故选C.
本题解析:
本题难度:一般
2、选择题 根据表中信息判断,下列选项不正确的是
序号
| 反应物
| 产物
|
①
| KMnO4、H2O2、H2SO4
| K2SO4、MnSO4
|
②
| Cl2、FeBr2
| FeCl3、FeBr3
|
③
| MnO4-
| Cl2、Mn2+
|
A.氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2
B.第①组反应的氧化产物为O2
C.第②组反应中参加反应的Cl2与 FeBr2的物质的量之比为1:2
D.第③组反应中生成1mol Cl2,转移电子2mol
参考答案:A
本题解析:A.根据①可知氧化性:MnO4->H2O2;根据②可知氧化性:Cl2>Br2>Fe3+;根据③可知氧化性:MnO4->Cl2,所以氧化性:MnO4->Cl2>Br2>Fe3+,错误;B.在第①组反应中氧化剂是KMnO4,还原剂是H2O2,氧化产物是O2,正确;C.第②组反应中3Cl2+ 6FeBr2= 2FeCl3+4FeBr3,所以Cl2与 FeBr2的的物质的量之比为1:2,正确;D.在第③组反应中根据电子转移数目相等可知:生成1mol Cl2,转移电子2mol,正确。
考点:考查氧化还原反应的有关知识。
本题难度:一般
3、选择题 反应(1)、(2)分别是从海藻灰和智利硝石中提取碘的主要反应:
2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2 (1)
2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2 (2)
下列说法正确的是?
[? ]
A.两个反应中NaHSO4均为氧化产物
B.I2在反应(1)中是还原产物,在反应(2)中是氧化产物
C.氧化性:MnO2>SO42- >IO3->I2
D.反应(1)、(2)中生成等量的I2时转移电子数之比为1:5
参考答案:D
本题解析:
本题难度:一般
4、填空题 在高温时,水蒸气与灼热的炭发生氧化还原反应的化学方程式是H2O+C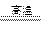 H2+CO,其中水是?剂。硫在氧气中燃烧的化学方程式是??,其中硫是?剂。
H2+CO,其中水是?剂。硫在氧气中燃烧的化学方程式是??,其中硫是?剂。
参考答案: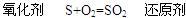
本题解析:略
本题难度:一般
5、填空题 (1)等物质的量的下列化合物与足量浓盐酸反应,得到氯气的物质的量最多的是
________(填序号)。
已知:MnO4-+H++Cl-
参考答案:
本题解析:
本题难度:一般