1、选择题 一定条件下进行反应A(g)?B(g)+xC(g),反应开始时容器中只含有A,其相对分子质量为32,平衡时混合气体的平均相对分子质量为20,此时A的转化率为30%,则x的值为( )
A.1
B.2
C.3
D.4
参考答案:反应开始时容器中只含有A,其相对分子质量为32,设A起始量为1mol,平衡时A的转化率为30%,
A(g)?B(g)+xC(g)
起始量(mol) 10 0
变化量(mol)0.3 0.3 0.3x
平衡量(mol) 0.7 0.3 0.3x
反应前后气体质量不变,混合气体的质量为32g,依据平均相对分子质量数值上等于平均摩尔质量的数值,
M=mn=32g0.7+0.3+0.3x=20
计算得到x=2
故选B.
本题解析:
本题难度:简单
2、选择题 在一定条件下发生反应 2A(g) === 2B(g)+C(g),将2 mol A通入2 L容积恒定的密闭容器甲中,若维持容器内温度不变,5 min末测得A的物质的量为0.8 mol。用B的浓度变化来表示该反应的速率为
[? ]
A.0.24 mol/(L・min)
B.0.08 mol/(L・min)
C.0.06 mol/(L・min)
D.0.12 mol/(L・min)
参考答案:D
本题解析:
本题难度:简单
3、填空题 某温度下,在一固定容积的容器中进行如下反应N2+3H2? ?2NH3,下列情况一定能说明反应已达到限度的是:?。(填序号)
?2NH3,下列情况一定能说明反应已达到限度的是:?。(填序号)
① 容器内气压不随时间变化? ② 1个N≡N键断裂的同时,有6个N―H键断裂
③?用N2、H2、NH3的物质的量浓度变化表示化学反应速率的比为1:3:2。
④ 容器内气体密度不再改变 ⑤ 混合气的平均相对分子质量不随时间变化
参考答案:1、2、5
本题解析:略
本题难度:简单
4、填空题 目前工业上有一种方法是用CO2来生产燃料甲醇。
CO2(g)+3H2(g)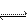 CH3OH(g)+H2O(g)?ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
CH3OH(g)+H2O(g)?ΔH=-49.0kJ/mol,为探究反应原理,现进行如下实验:
在体积为1 L的密闭容器中,充入1mol CO2和4 mol H2,一定条件下发生反应:测得CO2和CH3OH(g)的浓度随时间变化如图所示。

(1)从反应开始到平衡,氢气的平均反应速率v(H2)=?mol/(L・min)。
(2)该反应的平衡常数表达式为?。
(3)下列措施中能使n(CH3OH)/n(CO2)增大的是?。
A.升高温度
B.充入He(g),使体系压强增大
C.将H2O(g)从体系中分离
D.再充入1 mol CO2和4 mol H2
 mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为?。
mol CH3OH和1 mol H2O,为了使反应达到的化学平衡和上述一样,则起始还需加入H2的物质的量为?。