1������� ��������Ҫ�ɷ�ΪFeS2���ǹ�ҵ��ȡ�������Ҫԭ�ϣ������ղ���ΪSO2��Fe2O3��
��1����0.050mol SO2(g)��0.030mol O2(g)�����ݻ�Ϊ1L���ܱ������У���Ӧ��
2SO2(g)��O2(g) 2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040mol��L-1������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת����??��??��
2SO3(g)��һ�������´ﵽƽ�⣬���c(SO3)��0.040mol��L-1������������·�Ӧ��ƽ�ⳣ��K��SO2��ƽ��ת����??��??��
��2����֪������Ӧ�Ƿ��ȷ�Ӧ�����÷�Ӧ����ƽ��״̬ʱ�����������������£����д�ʩ�����������SO2ƽ��ת���ʵ���??������ĸ��ţ���ѡ���۷֣���
A�������¶�?B�������¶�
C������ѹǿ?D���������
E���Ƴ�����
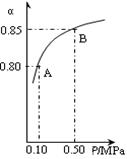
��3��ij�¶��£�������Ӧ��SO2��ƽ��ת���ʣ���������ϵ��ѹǿ��p���Ĺ�ϵ����ͼ��ʾ���жϣ�ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A)______K(B)�����������������������
2��ѡ���� ����ƽ����ϵ��mA������+ nB������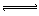 pC������+qD������+ Q�������жϣ�������ȷ����?
pC������+qD������+ Q�������жϣ�������ȷ����?
A�����¶Ȳ��䣬���������������1������ʱA��Ũ�ȱ�Ϊԭ����0.48������m+ n�� p+ q
B����ƽ��ʱ��A��B��ת������ȣ�˵����Ӧ��ʼʱ��A��B�����ʵ���֮��Ϊm��n
C����ƽ����ϵ��������a mol���������м���b mol B�������´ﵽƽ��ʱ������������ʵ������ڣ�a+b������m+n=p+q
D���¶Ȳ���ʱ����ѹǿ������ԭ����2�����ﵽ��ƽ��ʱ��
3��ѡ���� ���������У�����ȷ����(����)
A��ij�ض���Ӧ��ƽ�ⳣ�������¶ȵĺ���
B���������ܸı�ƽ�ⳣ���Ĵ�С
C��ƽ�ⳣ�������仯����ѧƽ��ض������ƶ����ﵽ�µ�ƽ��
D����ѧƽ�ⷢ���ƶ���ƽ�ⳣ���ط����仯
4������� (��12��) ���з�Ӧ��mA(g)��nB(g)? pC(g)���ﵽƽ��������¶�ʱ��B��ת���ʱ����Сѹǿʱ�������ϵ��C������������С����
(1)�÷�Ӧ���淴ӦΪ__________�ȷ�Ӧ����m��n________p(�>������������<��)��
(2)��ѹʱ��A����������________(���������С�����䡱����ͬ)��
(3)�����������ƽ��ʱ��������������ʵ���
________________________________________________________________________��
(4)��B����ɫ���ʣ�A��C����ɫ�������C(�������)ʱ�������ɫ________����ά��
������ѹǿ���䣬��������ʱ���������ɫ________(����������dz�����䡱)��
5������� ��֪���淴Ӧ��CO��g��+H2O��g��?CO2��g��+H2��s��������ij�¶��£���Ӧ�����ʼŨ�ȷֱ�Ϊ��c��CO��=1mol/L��c��H2O��=2.4mol/L���ﵽƽ���CO��ת����Ϊ60%��
��1�����ʱH2O��ת����Ϊ______�����¶��·�Ӧ��ƽ�ⳣ��Ϊ______��
��2������Ӧ�¶Ȳ��䣬��Ӧ�����ʼŨ�ȷֱ�Ϊ��c��CO��=4mol/L��c��H2O��=amol/L���ﵽƽ���c��CO2���T2mol/L����a����ֵΪ______��