1��ʵ���� ��10�֣�ij��ѧ��ѧʵ��С��Ϊ��֤���ͱȽ�SO2����ˮ��Ư���ԣ����������װ�ã�
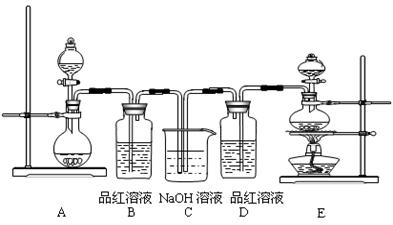
��1��ʵ���ҳ���װ��E�Ʊ�Cl2��ָ���÷�Ӧ��Ũ���������ֳ�������______��_______��?
��2����Ӧ��ʼ����B��D�����Թ��е�Ʒ����Һ����ɫ��ֹͣͨ����B��D�����Թܼ��ȣ������Թ��е�����ֱ�Ϊ��B ?�� D_________________��
��3��װ��C��������________________________________��
��4����ʵ��С��ļס�����λͬѧ��������������װ�ð���ͼװ�ü�������ʵ�飺
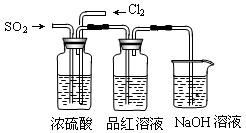
ͨ��һ��ʱ���ͬѧʵ�������Ʒ����Һ��������ɫ������ͬѧ��ʵ��������Ʒ����Һ��ʱ������Ʊ��Խ��Խdz��
�Ը��ݸ�ʵ��װ�ú�����ͬѧ��ʵ�����ش����⡣
���Է�����ͬѧʵ������У�Ʒ����Һ����ɫ��ԭ���ǣ�?
?��
������Ϊ��ͬѧ������������Ʒ����Һ���Խ��Խdz�ģ�
?
�ο��𰸣���10�֣���1�����ԣ�1�֣�����ԭ�ԣ�1�֣���
��2��B��Һ�ָ���ɫ��1�֣���? D��Һ����ɫ��1�֣�
��3�����ն����SO2��Cl2����ֹ��Ⱦ������2�֣�
��4���ٿ���SO2��Cl2�����ʵ���֮��1�U1���������߷�����Ӧ��������Ư���Ե�H2SO4��HCl��SO2 + Cl2 + 2H2O =SO42��+ 2Cl��+ 4H+ ��2�֣�
�ڿ���SO2��Cl2���������ʵ���,ʹ֮����ȣ�2�֣�
�����������
�����Ѷȣ�һ��
2��ѡ���� �о��л���һ�㾭�����¼����������裺���롢�ᴿ�� ȷ��ʵ��ʽ�� ȷ������ʽ�� ȷ���ṹʽ���������о��л���ķ����������
[? ]
A���������ڷ����ᴿҺ̬�л������
B���˴Ź�������ͨ�����ڷ����л������Է�������
C��ȼ�շ����о�ȷ���л���ɷֵ���Ч����֮һ
D�����л�����Ӻ������ͼ���о�������ȷ���л�������еĹ�����
�ο��𰸣�B
���������
�����Ѷȣ���
3��ѡ���� ijͬѧ��һС������ƺ�һ����Ƭ�ֱ���ڱ������У��о������ڿ����е��ȶ��ԡ���ѧ�����õ��о�������
[? ]
�ټ�˵�� ��ʵ�鷨 �۷��෨ �ܱȽϷ�
A���� ��
B���� ��
C���� ��
D���� ��
�ο��𰸣�C
���������
�����Ѷȣ���
4��ʵ���� (12��)����ȩ��һ�ֻ���ԭ�ϡ�ijʵ��С����������װ�úϳ�����ȩ�������ķ�Ӧ���£�
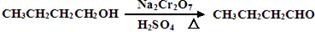 ����Ӧ��Ͳ������������б����£�
����Ӧ��Ͳ������������б����£�
?
| �е�/��
| �ܶ�/g��cm-3
| ˮ���ܽ���
|
������
| 117.2
| 0.8109
| ��
|
����ȩ
| 75.7
| 0.8017
| ��
|
ʵ�鲽�����£�
��Na2Cr2O7��Һ��Ũ������Һ������B�С���A�м����������ͼ�����ʯ�����ȣ����ַ�Ӧ�¶�Ϊ90��95�棬��E���ռ�90�����ϵ���֡�
������ﵹ���Һ©���У���ȥˮ�㣬�л������������ռ�75��77����֡�
�ش��������⣺

��1��ʵ���У��ܷ�Na2Cr2O7��Һ�ӵ�Ũ�����У�˵������?��
��2������װ��ͼ�У�B������������?��D������������?��
��3���¶ȼƵ����÷ֱ���C1?��C2?��
��4��������ȩ�ֲ�Ʒ���ڷ�Һ©����ˮ��?�㣨��ϡ����¡�����
��5����Ӧ�¶�Ӧ������90��95�棬��ԭ����?��
�ο��𰸣�����12�֣�ÿ��2�֣� ��1�����ܣ��ױŽ�?��2����Һ©��?������
��3��C1���Ʒ�Ӧ�¶ȣ�C2�ⶨ�������������¶�?��4����
��5���ȿɱ�֤����ȩ��ʱ�������ֿɾ��������䱻��һ������
�����������1����ΪŨ������ܶȴ�����ˮ���ȣ�����Na2Cr2O7��Һ�ӵ�Ũ�����У��������Ž���
�ʴ�Ϊ�����ܣ��������Ž���
��2�����������Ľṹ�ص��֪��B�����������ǵ�Һ©����D����������ֱ�������ܣ��ʴ�Ϊ����Һ©����ֱ�������ܣ�
��3�������¶ȼ�ˮ�����λ�ÿ�֪��C1���Ʒ�Ӧ�¶ȣ�C2�ⶨ�������������¶ȣ�
��4������ȩ�ܶ�Ϊ0.8017 g?cm-3��С��ˮ���ܶȣ��ʷֲ�ˮ�����·����ʴ�Ϊ���£�
��5��������Ŀ������Ӧ��Ͳ���ķе����ݿ�֪����Ӧ�¶ȱ�����90��95�棬�ȿɱ�֤����ȩ��ʱ�������ֿɾ��������䱻��һ���������ʴ�Ϊ����֤����ȩ��ʱ�������ֿɾ��������䱻��һ��������
�����Ѷȣ�һ��
5��ѡ���� ���������У����ϻ�ѧ��ѧ����
[? ]
A����������Ǽ�
B��������ˮΪ֮��������ˮ��˵����ͬ������ˮ�ͱ���ˮ��������
C���������������������������ܳɸ֡���˵���������ʵĻ�ѧ�仯��
D�������������Ϊͭ���еġ����ࡱ��ָ��ͭ
�ο��𰸣�B
���������
�����Ѷȣ���