1、填空题 (9分)日常生活中常见的金属材料有铝合金、钢铁等,某化学实验小组欲测定几种金属材料的耐腐蚀性,所用药品和试剂有:铝合金、钢铁、CO2、SO2、水。
(1)请完成以下实验设计表,并在实验目的的一栏中填入对应的实验编号:
实验编号
| 金属材料
| 溶?液
| 实验目的
|
①
| 铝合金
| CO2+ H2O
| Ⅰ.探究不同溶液对金属材料的腐蚀速率;
Ⅱ.探究不同金属材料的腐蚀速率;
|
②
| ?
| ?
|
③
| ?
| ?
|
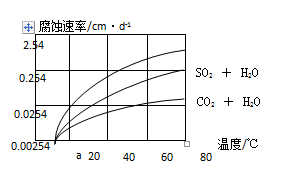
(2)在10%的盐酸中温度对铝合金的腐蚀速率影响关系见下图:铝合金在40℃时的腐蚀速率是20℃的?倍.

(3)请在上题图象中,画出铝合金在CO2溶液和SO2溶液中腐蚀速率随温度变化关系的预期结果示意图(都从a点开始)。
参考答案:(9分)(1)(2分/个)②铝合金? SO2+ H2O ?③?钢铁? CO2+ H2O?
?③?钢铁? CO2+ H2O?
(②钢铁? SO2+ H2O?③?钢铁? CO2+ H2O )
(2)10?(1分)
(3)(2分/个)
本题解析:略
本题难度:简单
2、填空题 (10分)
氯化亚铜(CuCl)是白色粉末,不溶于水、乙醇,熔点422℃,沸点1366℃,在空气中迅速被氧化成绿色,常用作有机合成工业中的催化剂。以粗盐水(含Ca2+、Mg2+、SO2-4等杂质)。Cu、稀硫酸,SO2等为原料合成CuCl的工艺如下:
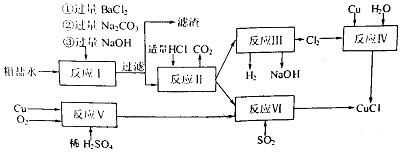
(1)反应I中加Na2CO3溶液的作用是?。
过一步反(2)反应II在电解条件下进行,电解时阳极发生的电极反应可表示为?。
(3)写出反应VI的化学方程式?。
(4)反应IV加入的Cu必须过量,其目的是?。
(5)反应VI后,过滤得到CuCl沉淀,用无水乙醇洗涤沉淀,在真空干燥机内于70℃干燥2小时,冷却,密封包装即得产品。于70℃真空干燥的目的是?。
参考答案:(1)除去Ca2+和过量的Ba2+
(2)2Cl―2e-=Cl2↑
(3)2CuSO4+2NaCl+SO2+2H2O=2CuCl↓+2NaHSO4+H2SO4
或2CuSO4+2NaCl+SO2+2H2O=2CuCl↓+Na2SO4+2H2SO4
(4)防止生成CuCl2
(5)加快乙醇和水的蒸发,防止CuCl被空气氧化
本题解析:略
本题难度:一般
3、选择题 下列实验装置设计正确,且能达到目的的是
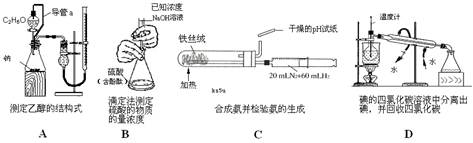
参考答案:A
本题解析:B不正确,氢氧化钠溶液应该盛放在碱式滴定管中;pH试纸检验氨气的性质,试纸应该是湿润的;蒸馏时温度计水银球应该放在蒸馏烧瓶支管出口处,D不正确,答案选A。
本题难度:简单
4、实验题 Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计] 控制p - CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
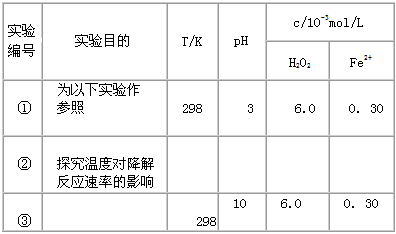
[数据处理] 实验测得p - CP的浓度随时间变化的关系如下图。
|

(2)请根据上图实验①曲线,计算降解反应50~150s内的反应速率:
v(p - CP)=_________mol・L-l・s-l
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从
Fenton法所用试剂H2O2的角度分析原因:____________________________
(4)实验③得出的结论是:pH等于10时,____________________________。
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:_______________________________。
参考答案:(1)②313;3;6.0;0. 30;③探究溶液的pH对降解反应速率的影响
(2)8.0×10-6
(3)过氧化氢在温度过高时迅速分解
(4)反应速率趋向于零(或该降解反应趋于停止)
(5)将所取样品迅速加入到一定量的NaOH溶液中,使pH约为10(或将所取样品骤冷,答案合理即可)
本题解析:
本题难度:困难
5、选择题 下列实验能达到目的的是?(?)
A.分别加热蒸干灼烧NaAlO2溶液和AlCl3溶液,最终都能得到Al2O3
B.在滴有酚酞的Na2CO3溶液中,加入BaCl2溶液后红色褪去,验证Na2CO3溶液中存在水解平衡
C.检验Fe2O3中是杏含有FeO,用盐酸溶解样品后,滴加高锰酸钾溶液,观察溶液紫色是否褪色或变浅
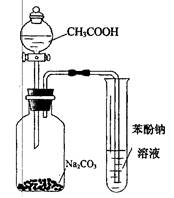
D.利用图示装置并根据有关实验现象能推知酸性: CH3COOH>H2CO3>C6H2OH
参考答案:B
本题解析:略
本题难度:一般