1、选择题 把a、b、c、d四块金属浸泡在稀H2SO4中,用导线两两相连可组成原电池。若a、b相连时,a为负极;c、d相连时,c为负极,a、c相连时,c为正极,b、d相连时,b为正极。则这四种金属的活泼性顺序由大到小为( )
A.a>b>c>d
B.a>c>d>b
C.c>a>b>d
D.b>d>c>a
参考答案:B
本题解析:若a、b相连时,a为负极即活动性:a>b;c、d相连时,c为负极,即c>d;a、c相连时,c为正极,即a>c;,b、d相连时,b为正极,即b>d;综上所述,四种金属的活泼性顺序由大到小为a>c>d>b,即B正确;
本题难度:简单
2、简答题 (9分)下图是某化学兴趣小组探究不同条件下化学能转变为电能的装置。
请回答下列问题:
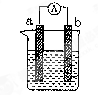
(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,正极的电极反应式为:?。
(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该装置?
(填“能”或“不能”)形成原电池,若不能,请说明理由;若能,请指出正、负极材料:?。当反应中收集到标准状况下224mL气体时,消耗的电极质量为?g。
(3)燃料电池的工作原理是将燃料和氧化剂(如O2)反应所产生的化学能直接转化为电能。现设计一燃料电池,以电极a为正极,电极b为负极,甲烷为燃料,采用氢氧化钠溶液为电解液;则甲烷应通入?极(填a或b,下同),电子从 ?极流出,电解质溶液中OH-向?极移动。
参考答案:(1)2H++2e-=H2↑;(2)能,镁(或b)为正极,铝(或a)为负极;0.18;(3)b;b;b
本题解析:(1)当电极a为Al,电极b为Cu,电解质溶液为稀硫酸时,由于活动性Al>Cu.所以Al为负极。Cu为正极。在正极的电极反应式为:2H++2e-=H2↑;(2)当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,由于Al能与NaOH溶液发生氧化还原反应,所以该装置能够形成原电池。Al为负极;Mg为正极。反应的总方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑。n(H2)=0.224L÷22.4L/mol=0.01mol,所以根据方程式中Al的质量为2/3×0.01mol×27g/mol="0.18g." (3)该电池为甲烷燃料电池,通入甲烷的电极为负极,通入氧气的电极为正极。由于电极a为正极,电极b为负极,所以b电极通入甲烷,电子从电源的负极流出,经用电器流回到正极。因此电子从负极b流出,在电解质溶液中,根据同种电荷相互排斥,异种电荷相互吸引的原则,电解质溶液中OH-向正电荷较多的负极b移动。
本题难度:一般
3、选择题 按下图装置实验,若x轴表示流入正极的电子的物质的量,忽略溶液体积的变化;则y轴应表示

①c(Ag+)? ②c(NO3-)? ③a棒的质量?
④b棒的质量? ⑤溶液的质量
A.①②③
B.②③⑤
C.①②④
D.仅②
参考答案:D
本题解析:在原电池中较活泼的金属作负极,铁比银活泼,所以铁是负极,失去电子,即a棒质量减小。银是正极,溶液中的银离子在正极得到电子而析出,即b棒质量增加。根据图像可知,随着反应的进行,y是不变的,所以不变的是NO3-的浓度,答案选D。
本题难度:简单
4、选择题 有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸溶液中,A为负极;②C、D用导线相连后,同时浸入稀硫酸溶液中,电流由D→导线→C;③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀硫酸溶液中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。据此,判断五种金属的活动性顺序是
A.A>B>C>D>E B.A>C>D>B>E
C.C>A>B>D>E D.B>D>C>A>E
参考答案:B
本题解析:①A、B用导线相连后,同时浸入稀硫酸溶液中,A极为负极,所以活泼性:A>B;②原地啊池中,电流从正极流向负极,C、D用导线相连后,同时浸入稀硫酸溶液中,电流由D→导线→C,所以金属活泼性:C>D;③A、C相连后,同时浸入稀硫酸溶液中,C极产生大量气泡,说明C极是正极,所以金属活泼性:A>C;④B、D相连后,同时浸入稀硫酸溶液中,D极发生氧化反应,说明D极是负极,所以金属活泼性:D>B;综上可知金属活泼性顺序是:A>C>D>B.答案选B.
考点:原电池原理
本题难度:一般
5、选择题 下列关于原电池和电解池的说法正确的是( )
A.

如图所示,把盐桥换为铜导线也可以形成原电池
B.电解饱和食盐水制烧碱,用碳钢网作阳极
C.白铁是在铁上电镀锌,用锌作阳极,铁作阴极
D.电解法精炼粗铜时,电解质溶液CuSO4溶液浓度不变
参考答案:A、把盐桥换为铜导线,硫酸铜溶液的烧杯中无氧化还原反应,硫酸亚铁溶液的烧杯中无自发进行的氧化还原反应,不能形成原电池,故A错误;
B、电解饱和食盐水制烧碱,用碳钢网作阳极,铁失电子生成亚铁离子结合阴极附近氢氧根形成沉淀,不能制的氢氧化钠,故B错误;
C、镀原理是镀层金属做阳极,待镀金属做阴极;白铁是在铁上电镀锌,用锌作阳极,铁作阴极,故C正确;
D、电解法精炼粗铜时,阳极失电子的除铜外,铁、镍、锌等也失电子,电解质溶液CuSO4溶液浓度发生改变,故D错误;
故选C.
本题解析:
本题难度:简单