| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《原电池原理》高频试题预测(2020年最新版)(十)
参考答案:D 本题解析:A.放电时,Fe是负极,发生氧化反应,NiO2是正极,发生还原反应,原说法错误;B.因为是碱性电池,蓄电池的电极不可以浸入某种酸性电解质溶液中,原说法错误;C.放电时,电解质溶液中的阴离子向负极(负极失去电子,带正电荷)方向移动,原说法不正确;D.充电时,阴极上的电极反应式为:Fe(OH)2+2e-=Fe+2OH-,正确。 本题难度:一般 2、选择题 气体的自动化检测中常常应用原电池原理的传感器。下图为电池的工作示意图:气体扩散进入传感器,在敏感电极上发生反应,传感器就会接收到电信号。下表列出了待测气体及敏感电极上部分反应产物。则下列说法中正确的是 |
参考答案:D
本题解析:A、原电池中的正极发生还原反应,得到电子,元素的化合价降低,而待测气体为CO时,反应产物为二氧化碳,C元素的化合价升高,发生氧化反应,所以此时敏感电极作负极,同理,待测气体为硫化氢时,S元素的化合价也升高,敏感电极作负极,错误;B、H2S和CO体积分数相同也即物质的量相同,而等物质的量的二者失去的电子的物质的量不同,CO失去2个电子,而硫化氢中S则失去8个电子,所以在气体的扩散速度相同的前提下,传感器上产生的电流大小不同,错误;C、检测H2S时,因为电极产物为硫酸,所以电解质溶液为硫酸,对电极为正极,发生还原反应,充入空气,则正极发生的反应是氧气得到电子,与氢离子结合为水,错误;D、检测Cl2时,Cl元素的化合价降低,所以敏感电极作正极,则敏感电极的反应是:Cl2 + 2e-= 2Cl-,正确,答案选D。
考点:考查原电池反应原理的应用
本题难度:一般
3、选择题 如图所示是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,在读书卡上的记录如下,则卡片上的描述合理的是( )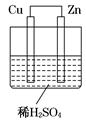
| 卡片号:2 2013.3.15,实验后的记录: ①Cu为负极,Zn为正极 ②Cu极上有气泡产生 ③SO42 |
参考答案:
本题解析:
本题难度:一般
4、填空题 (14分)短周期主族元素A、B、C、D、E原子序数依次增大 , A是元素周期表中原子半径最小的元素,B是形成化合物种类最多的元素,C原子的最外层电子数是次外层电子数的3倍,D是同周期中金属性最强的元素,E的负一价离子与C的某种氢化物分子含有相同的电子数。
⑴A、C、D形成的化合物中含有的化学键类型为 。
⑵已知:
① E-E→2E ?H=+a kJ/mol;
② 2A→A-A ?H=-b kJ/mol;
③ E+A→A-E ?H=-c kJ/mol;
写出298K时,A2与E2反应的热化学方程式 。
⑶在某温度下容积均为2 L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2A2(g)+BC(g) X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
X(g) ?H=-Q kJ/mol(Q>0,X为A、B、C三种元素组成的一种化合物)。初始投料与各容器达到平衡时的有关数据如下:
| 实验 | 甲 | 乙 | 丙 |
| 初始投料 | 2 mol A2、1 mol BC | 1 mol X | 4 mol A2、2 mol BC |
| 平衡时n(X) | 0.5 mol | n2 | n3 |
| 反应的能量变化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 体系的压强 | P1 | P2 | P3 |
| 反应物的转化率 | 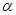 1 1 | 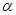 2 2 | 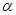 3 3 |
参考答案:⑴离子键、极性键(或共价键)
⑵ H2(g)+Cl2(g)=2HCl(g) ?H=(a+b-2c)kJ・mol-1[?H表示成-(2c-a-b)kJ・mol-1也可]
⑶①0.125 mol・L-1・min-1
②4 L2/mol2 ③ ABD
④
⑷ O2+4e-+2CO2=2CO32-
本题解析:根据题意依次推出A为氢元素,B为碳元素,C为氧元素,D为钠元素,E为氯元素;
⑴A、C、D形成的化合物为NaOH,其所含化学键为离子键、极性键(或共价键);
⑵首先写出A2与E2反应的方程式,并标出各物质的状态为H2(g)+Cl2(g)=2HCl(g);将“①-②+③×2”得该化学方程式,根据盖斯定律得该反应热?H=(a+b-2c)kJ・mol-1,据此便可写出完整的热化学方程式;
⑶①A2的平均反应速率v (A2)=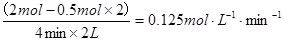 ;
;
②该温度下此反应的平衡常数K=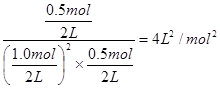 ;
;
③甲和乙两容器的平衡状态为全等平衡,则有α1+α2=1,Q1+Q2=Q,P1=P2,n2=n1=0.5 mol;由于丙容器的起始量是甲的2倍,可将丙容器的体积扩大2倍(与甲同压等效),然后再恢复到原体积,则可得α3>α1,P3<2P1,n2<1.0 mol<n3,Q3>2Q1,综上只有A、B、D项正确。
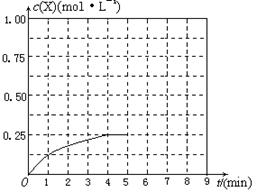
④第5min时X的物质的量浓度变为0.5 mol/L(体积变为1 L),再根据“第8min达到新的平衡时A2的总转化率为75%”,则到新平衡时X的物质的量浓度为 ,据此便可作图。
,据此便可作图。
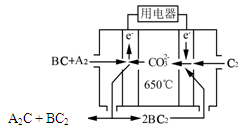
⑷O2在正极上发生还原反应生成CO32-:O2+4e-+2CO2=2CO32-。
考点:本题考查化学与热量、化学反应速率与化学平衡常数、等效平衡、电化学等。
本题难度:困难
5、选择题 某课外活动小组使用下列用品设计原电池。用品:铜片、铁片、导线、金属夹、发光二极管、果汁(橙汁、苹果汁)500mL,、烧杯。下列说法正确的是
A.该装置能将电能转化为化学能 B.实验过程中铜片逐渐溶解
C电子由铁片通过导线流向铜片 D.铁片上会析出红色的铜
参考答案:C
本题解析:略
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《物质的分离.. | |