1、实验题 碱式碳酸铜可表示为:xCuCO3・yCu(OH)2・zH2O,测定碱式碳酸铜组成的方法有多种(Cu
的相对原子质量按63.5计)。
(1)现采用氢气还原法,请回答下列问题:
已知xCuCO3・yCu(OH)2・zH2O与氢气反应的化学方程式为xCuCO3・yCu(OH)2・zH2O+(x+y)H2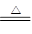 (x+y)Cu+xCO2+(x+2y+z)H2O
(x+y)Cu+xCO2+(x+2y+z)H2O
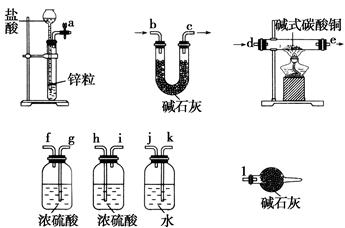
①实验装置用下列所有仪器连接而成,按氢气流方向的连接顺序是(填入仪器接口字母编号):
(a)→( )( )→( )( )→( )( )→( )( )→( )( )→(l);
②称取23.9 g某碱式碳酸铜样品,充分反应后得到12.7 g残留物,生成4.4 g二氧化碳和7.2 g水。该样品的结晶水质量为________g,化学式为________。
(2)某同学以氮气代替氢气,并用上述全部或部分仪器来测定碱式碳酸铜的组成,你认为是否可行?请说明理由_________________________________________________________
参考答案:(1)①k j g(或h) f(或i) d e h(或g) i(或f) b c
②1.8 CuCO3・Cu(OH)2・H2O
(2)可行。根据反应xCuCO3・yCu(OH)2・zH2O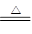 (x+y)CuO+xCO2↑+(y+z)H2O↑,依据碱式碳酸铜、CuO、CO2和H2O的质量(或其中任意三个量),即可计算出其组成
(x+y)CuO+xCO2↑+(y+z)H2O↑,依据碱式碳酸铜、CuO、CO2和H2O的质量(或其中任意三个量),即可计算出其组成
本题解析:(1)①由实验目的和实验装置知,该实验要测定生成的水、二氧化碳的量,而从a口出来的氢气中含有水蒸气和挥发出来的氯化氢,会对实验有干扰,所以应先用水吸收氯化氢,再用浓硫酸吸收水蒸气,再通入碱式碳酸铜中发生反应,而产生的两种气体应先用浓硫酸吸收水蒸气,再用U形管中的碱石灰吸收二氧化碳,同时要连接上装有碱石灰的球形干燥管,防止空气中的水蒸气和二氧化碳进入U形管而产生误差。②根据所给数据可计算出生成的铜、二氧化碳、水的物质的量分别为0.2 mol、1 mol、0.4 mol,所以可知(x+y)∶x∶(x+2y+z)=2∶1∶4,故x、y、z分别为1、1、1,从而求得碱式碳酸铜样品的化学式及结晶水的质量。
(2)若以氮气代替氢气,则原理是利用碱式碳酸铜热分解的化学方程式:
xCuCO3・yCu(OH)2・zH2O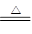 (x+y)CuO+xCO2↑+(y+z)H2O↑,要想完成实验目的,知道碱式碳酸铜、CuO、CO2和H2O的质量(或其中任意三个量)即可。
(x+y)CuO+xCO2↑+(y+z)H2O↑,要想完成实验目的,知道碱式碳酸铜、CuO、CO2和H2O的质量(或其中任意三个量)即可。
本题难度:一般
2、选择题 .取含有Fe2O3杂质的铁粉100g,投入过量的盐酸中,产生H2标准状况下31.36L,在反应后的溶液中加入KSCN溶液,没有红色产生,问样品中杂质含量(?)
A? 4%? B? 32%? C? 8%? D? 16%
参考答案:D
本题解析:氢气是1.4mol,所以和盐酸反应生成氢气的铁是1.4mol。设氧化铁的物质的量是x,则氯化铁就是2x,所以和氯化铁反应的铁是x,因此有160x+(x+1.4)×56=100,解得x=0.1mol,所以杂的含量是160x÷100,即16%,答案选D。
本题难度:一般
3、选择题 下列有关实验原理或操作不正确的是( )
A.镀锌铁皮镀锌层厚度的测定:用1:4的硫酸溶液与镀锌铁皮反应,当产生的氢气速率明显减慢时,锌镀层完全反应
B.乙醇与浓硫酸共热至170℃,将制得的气体通入酸性KMnO4溶液来检验制得气体是否为乙烯
C.阿司匹林的提纯是将粗产品先溶解在饱和碳酸氢钠溶液中,过滤后向滤液加入盐酸,冷却后有晶体析出,抽滤并用少量的冷水洗涤晶体
D.用盐酸检验牙膏中的摩擦剂是SiO2、CaCO3、Ca3(PO4)2中的哪一种
参考答案:B
本题解析:
本题难度:简单
4、填空题 某地产孔雀石的主要成分是Cu3(OH)4CO3。
(1)试写出该孔雀石高温分解的化学方程式:_________________________________。
(2)试以(1)中所得金属氧化物为原料,分别采用湿法冶炼和高温冶炼的方式制取金属铜。供选择的试剂有:①木炭②铁屑③生石灰④稀H2SO4,不得另选其他试剂,写出反应的化学方程式。
A.湿法冶炼:___________、___________(可不填满,也可补充。下同)
B.高温冶炼:___________、___________。
参考答案:(1)Cu3(OH)4CO3 3CuO+2H2O↑+CO2↑
3CuO+2H2O↑+CO2↑
(2)A.CuO+H2SO4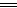 CuSO4+H2O? Fe+CuSO4
CuSO4+H2O? Fe+CuSO4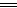 FeSO4+Cu
FeSO4+Cu
B.2CuO+C 2Cu+CO2↑(或CuO+C
2Cu+CO2↑(或CuO+C Cu+CO↑)
Cu+CO↑)
本题解析:湿法冶金术和热还原冶炼法
本题难度:简单
5、选择题 向200ml 0.1mol/L的FeCl2溶液中加入适量的NaOH溶液,使Fe2+恰好完全沉淀,过滤,小心加热沉淀,直到水分蒸干,再灼烧到质量不再变化,此时固体的质量为
A.1.14g
B.1.6g
C.2.82g
D.4.36g
参考答案:B
本题解析:略
本题难度:一般