1、选择题 欲使0.1mol/L的NaHCO3溶液中c(H+)、c(CO32-)、c(HCO3-)都减少,其方法是
[? ]
A.通入二氧化碳气体
B.加入氢氧化钠固体
C.通入氯化氢气体
D.加入饱和石灰水
参考答案:D
本题解析:
本题难度:一般
2、选择题 有下列四种溶液:①盐酸;②氯化铁;③氢氧化钠;④碳酸钠。它们的pH分别为4,4,10,10,溶液中水的电离度为α1,α2,α3,α4,则下列关系正确的是
A.α1=α2>α3=α4
B.α2=α4>α1=α3
C.α1=α2=α3=α4
D.α1=α3>α2=α4
参考答案:B
本题解析:反应H2O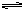 H++OH--Q;①向水中加入酸或碱,[H+]或[OH-]增大,平衡向左移动,抑制了水的电离,αH2O减小;②向水中加入能水解的盐,消耗H+或OH-,使平衡向右移动,促进水的电离,αH2O增大;③升高温度,平衡向右移动,αH2O增大;④向水中加入其他能与H+或OH-反应的物质,也能促进水的电离。如Na2O,Na等。题中给出了四种溶液的溶质及pH,要求排列电离度α的顺序。只要表示出水电离出来的[H+]水或[OH-]水,然后直接比较其大小即可。
H++OH--Q;①向水中加入酸或碱,[H+]或[OH-]增大,平衡向左移动,抑制了水的电离,αH2O减小;②向水中加入能水解的盐,消耗H+或OH-,使平衡向右移动,促进水的电离,αH2O增大;③升高温度,平衡向右移动,αH2O增大;④向水中加入其他能与H+或OH-反应的物质,也能促进水的电离。如Na2O,Na等。题中给出了四种溶液的溶质及pH,要求排列电离度α的顺序。只要表示出水电离出来的[H+]水或[OH-]水,然后直接比较其大小即可。
pH=4的盐酸:OH-为水电离产生的,[OH-]水=10-10mol/L
pH=4的FeCl3溶液,H+为水电离出来的,[H+]水=10-4mol/L
pH=10的Na2CO3溶液,OH-为水电离出来的,[OH-]=10-4mol/L
pH=10的NaOH溶液,H+为水电离出来的,[H+]=10-10mol/L
所以B的顺序是正确的。
本题难度:一般
3、选择题 在25 ℃时,将pH = 11的NaOH溶液与pH = 3的CH3COOH溶液等体积混合后,下列关系式中正确的是 (? )
A.c(Na+) = c(CH3COO-)+c(CH3COOH)
B.c(H+) = c(CH3COO-)+c(OH-)
C.c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
D.c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
参考答案:D
本题解析:将pH = 11的NaOH溶液与pH = 3的CH3COOH溶液等体积混合后,因为碱中c(OH-)与酸中c(H+)相等,等体积混合后,因CH3COOH是弱酸,会大量的剩余,所以反应后溶液显酸性,c(H+)>c(OH-),C错。反应后的溶质为大量的CH3COOH,少量的CH3COONa。所以c(Na+) <c(CH3COO-)+c(CH3COOH),A错。根据电荷守恒得c(Na+) + c(H+) = c(CH3COO-)+c(OH-),B错。故选D
本题难度:一般
4、选择题 50℃时,下列各溶液中,离子的物质的量浓度关系正确的是
A.饱和纯碱(Na2CO3)溶液中:c(Na+)=2c(CO32-)
B.pH=4的醋酸中:c(H+)=1.0×10-4mol・L-1
C.0.10mol/L醋酸钠溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
D.pH=12的纯碱溶液中:c(OH-)=1.0×10-2mol・L-1
参考答案:BC
本题解析:A、碳酸钠溶于水CO32-水解,因此在碳酸钠溶液中c(Na+)>2c(CO32-),A不正确;B、溶液中氢离子浓度的负对数等于pH,因此pH=4的醋酸中:c(H+)=1.0×10-4mol・L-1,B正确;C、根据电荷守恒可知,在0.10mol/L醋酸钠溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(OH-),C正确;D、水的离子积常数受温度影响,因此在不能确定溶液温度的条件下,无法计算pH=12的纯碱溶液中c(OH-),只能得出c(H+)=1.0×10-12mol・L-1,D不正确,答案选BC。
本题难度:一般
5、选择题 为了除去氯化镁酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种过量的试剂,过
滤后再加入适量的盐酸。这种试剂是
A.氨水
B.氢氧化钠
C.碳酸镁
D.碳酸钠
参考答案:C
本题解析:除杂的原则是“不增、不减”。即不增加新的杂质,不减少被提纯的物质本身。由于是除去氯化镁酸性溶液中的Fe3+,可在加热搅拌的条件下加入一种过量的含有Mg元素的物质,既能反应消耗酸,使溶液的PH增大,以除去杂质Fe3+,也不添加新的杂质。分析各个选项,只有C. 碳酸镁符合要求。
本题难度:一般