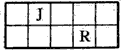
1、填空题 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如右表; J元素最低负化合价的绝对值与其原子最外层电子数相等;M是地壳中含量最多的金属元素。
(1)M的离子结构示意图为______;元素T在周期表中位于第______族。
(2)J和氢组成的化合物分子有6个原子,其结构简式为____。
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为____________。
(4)L的最简单气态氢化物甲的水溶液显碱性。 ①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,其化学方程式为____________________。
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,仅改变下表中反应条件x,该平衡体系中随x递增y递减的是____________(选填序号)。

(5)由J、R形成的液态化合物JR2 0.2 mol在O2中完全燃烧,生成两种气态氧化物,298 K时放出热量215 kJ。该反应的热化学方程式为____。
参考答案:(1)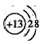 ;ⅦA
;ⅦA
(2) CH2=CH2
(3) AlCl3+3H2O=Al(OH)3+3HCl↑
(4)①2NH3・H2O+3H2O2==N2↑+8H2O(或2NH3+3H2O2==N2↑+6H2O); ②a和c(或a或c)
(5)1/5CS2(1)+3/5O2(g)==1/5CO2(g)+2/5SO3(g) △H=-215kJ・mol-1
本题解析:
本题难度:一般
2、选择题 X、Y均为短周期元素,X位于IA族,X、Y能形成X2Y型化合物,下列说法中正确的是
[? ]
A.X与Y形成的化合物中原子个数比可能为1:1
B.X2Y不可能是共价化合物
C.X和Y分别形成的简单离子不可能具有相同电子层结构
D.根据周期表递变规律判断X原子半径一定大于Y原子半径
参考答案:A
本题解析:
本题难度:简单
3、选择题 下列各组元素原子第一电离能I1的递增的顺序正确的为
A.BB.He
参考答案:A
本题解析:试题分析:非金属性越强,第一电离能越大,A正确;B不正确,应该是He>Ne>Ar;C不正确,应该是Si<As<P;D不正确,应该是Na<Al<Mg,答案选A。
考点:考查第一电离能的大小判断
点评:该题是基础性试题的考查,试题难易适中,侧重对学生能力的培养。该题的关键是明确影响第一电离能大小的因素,特别还要注意的是共性与个性的关系,有助于培养学生的逻辑推理能力和灵活应变能力。
本题难度:困难
4、选择题 电子层数相同的短周期元素X、Y、Z、W,其中X的最外层电子数比K层少1,Y的最外层电子数比K层多l,Z的单质是一种半导体材料,常用于制造太阳能电池,W的原子半径?是同周期中最小的.下列推断中正确的是( )
A.Z的氢化物的热稳定性强于w的氢化物
B.Z的氧化物与水反应可制得相应的含氧酸
C.X、Y、W的原子半径依次减小,对应的离子半径依次增大
D.X、Y、W的最高价氧化物对应水化物之间互相都能发生反应
参考答案:电子层数相同的短周期元素X、Y、Z、W,;Z的单质是一种半导体材料,常用于制造太阳能电池,Z为Si;X的最外层电子数比K层少1,则X为Na;Y的最外层电子数比K层多l,则Y为Al
W的原子半径是同周期中最小的,则W为Cl,
A.非金属性Cl>Si,则W的氢化物的热稳定性强于Z的氢化物,故A错误;
B.二氧化硅不与水反应,故B错误;
C.Na、Al、Cl在同周期,原子半径在碱小,氯离子的半径最大,铝离子半径最小,故C错误;
D.X、Y、W的最高价氧化物对应水化物分别为NaOH、Al(OH)3、HClO4,Al(OH)3具有两性,则水化物之间互相都能发生反应,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 对于IVA族元素,下列叙述中不正确的是( )
A.SiO2和CO2中,Si和O、C和O之间都是共价键
B.Si、C、Ge的最外层电子数都是4,次外层电子数都是8
C.SiO2和CO2中都是酸性氧化物,在一定条件下都能和氧化钙反应
D.该族元素的主要化合价是+4和+2
参考答案:A、共价化合物中非金属元素之间以共价键结合,故A正确;
B、最外层都是4没错,但是C此外层不是8,故B错误;
C、酸性氧化物和碱性氧化物一定条件可以反应,故C正确;
D、碳族元素的最外层电子数为4,所以最高正价为+4价,当然也能形成+2价,故D正确;
故选:B.
本题解析:
本题难度:简单