1、填空题 某化学兴趣小组进行如下图所示的电化学实验,实验前查资料获知:铁氰化钾(K3[Fe(CN)6])遇Fe2+产生 蓝色沉淀。V形管以多孔Pt为电极;U形管A端滴入1~2滴K3[Fe(CN)6]溶液。
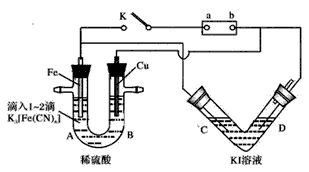
(1)开始时,接通K电键:U形管中无沉淀,却观察到B端____;根据以上实验可知电源正极为____(填“a”或“b”)。Fe电极上发生的电极反应为___,V形管中现象是___ 。
(2)断开K电键,U形管中现象:A端___;B端____,B端有关反应方程式为____。V形管中现象与(1)的____(填“相同”或“不同”)。
参考答案:(1)溶液变蓝色; b; 2H++2e-==H2↑ ;C端产生无色气体,D 端溶液变橙黄,C端液面低于D端液面
(2)产生蓝色沉淀; 溶液颜色变浅,产生无色气体(H2) ;Cu2++2e-==Cu、2H++2e-==H2↑? ;相同
本题解析:
本题难度:一般
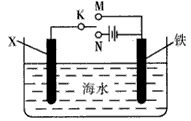
2、选择题 下图是模拟电化学反应的装置图。下列说法正确的是
[? ]
A.若X为碳棒,开关K置于N处,可以减缓铁的腐蚀
B.若X为碳棒,开关K置于M处,则铁电极的电极反应式为Fe - 3e - ==Fe3+
C.若X为锌,开关K置于N处,则X极减少的质量与铁电极增加的质量相等
D.若X为锌,开关K置于M处,则总反应方程式为2Fe +O2+2H2O==2Fe(OH)2
参考答案:A
本题解析:
本题难度:一般
3、填空题 下图是某同学自己设计的装置:用大塑料瓶子截去瓶底,留瓶口一段约8cm~10cm,瓶口配一胶塞由里向外塞紧。A、B两极是用镀铬曲别针伸直做成,由塞子露头处连接导线。试回答:其所用电源为 电,由图可知A端为 极;与A端相连接的试管中得到的气体是 ,可用 来检验。
参考答案:直流电 正极;氧气 带火星的木条
本题解析:本题是一道电解水的综合题,它既涉及电解水电源的选择、电极的确定,还涉及到气体的确定和检验。解题时首先应分析图中信息(A端产生气体体积少),得出A端汇集的是氧气结论后(正、氧、少;负、氢、多)。方能正确解答本题。
本题难度:简单
4、填空题 已知甲池的总反应式为: 2CH3OH+3O2+4KOH 2K2CO3+6H2O
(1)请回答图中甲、乙两池的名称。

甲池是 装置;乙池是 装置。
(2)请回答下列电极的名称:通入CH3OH的电极名称是 ,B(石墨)电极的名称是 。
(3)写出电极反应式:通入O2的电极的电极反应式是 。
(4)乙池中反应的化学方程式为 。
(5)当乙池中A(Fe)极的质量增加5.40g时,甲池中理论上消耗O2 mL(标准状况下)
参考答案:(1)原电池(化学能转变为电能) 电解池(电能转变为化学能)
(2)负极 阳极
(3)O2+2H2O+4e-=4OH-
(4)4AgNO4+2H2O=4Ag+O2↑+4HNO3
(5)280
本题解析:(1)由装置图可以看出甲池为原电池,乙池是电解池。(2)通入燃料CH3OH的电极名称是负极,通入氧气的电极为正极。在乙池中与电源的正极相连接的石墨电极B为阳极。与电源的负极相链接的Fe电极为阴极。(3)在原电池中,负极发生氧化反应。正极上发生还原反应。由于是碱性环境,所以在通入O2的电极即正极的电极反应式是O2+2H2O+4e-=4OH-。(5)由于在整个闭合回路中电子转移的数目相等。所以当乙池中A(Fe)极的质量增加5.40g时,n(Ag)=n(e-)=5.40g÷107g/mol=0.05mol.则n(O2)= 0.05mol÷4=0.0125mol.所以V(O2)= 0.0125mol×22.4L/mol=0.28L=280ml。
考点:考查原电池、电解池的工作原理、电极名称、电极反应、电子转移及有关计算的知识。
本题难度:一般
5、选择题 用惰性电极电解物质的量浓度均为0.2 mol/L NaCl和CuSO4的混合液200 mL,经一段时间后,阴极上得到896 mL (标准状况下)的气体,则阳极收集到气体的体积为(标准状况、不考虑气体的溶解)
A.672 mL
B.896 mL
C.1120 mL
D.1344mL
参考答案:C
本题解析:惰性电极电解NaCl和CuSO4的混合液,阳极首先是氯离子放电,发生氧化反应,生成氯气,如果氯离子不足,溶液中的OH-再放电,生成氧气。阴极首先是铜离子放电,发生还原反应生成铜,如果铜离子不足,溶液中的氢离子再放电,生成氢气。阴极上得到896 mL (标准状况下)的气体,说明铜离子不足,所以阴极共转移的电子是0.2mol/L×0.2L×2+ =0.16mol。阳极氯离子失去的电子是0.2mol/L×0.2L×1=0.04mol,根据得失电子守恒可知氧气的物质的量是
=0.16mol。阳极氯离子失去的电子是0.2mol/L×0.2L×1=0.04mol,根据得失电子守恒可知氧气的物质的量是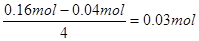 ,所以氧气和氯气的体积是0.05mol/L×22.4L/mol=1.12L,所以答案是C。
,所以氧气和氯气的体积是0.05mol/L×22.4L/mol=1.12L,所以答案是C。
本题难度:一般