|
高中化学知识点讲解《化学平衡常数》考点预测(2020年强化版)(四)
2021-06-11 06:39:55
【 大 中 小】
|
1、选择题 反应A(s)+a?B(g)=b?C(g)达到平衡时,温度和压强对该反应yP2P1速率的影响如图所示,图中P1>P2,x轴表示温度,y轴表示平衡混合气体中B的体积分数.有下列判断,其中正确的是( )
①正反应是放热反应;?②正反应是吸热反应;? ③a>b;?④a<b.
A.①③
B.②④
C.②③
D.①④
| 
参考答案:B
本题解析:
本题难度:简单
2、简答题 一定温度下,在2L的密闭容器中X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,依据题意,回答下列问题.(1)反应开始到10s,用Z表示的反应速率为______;
(2)反应达到平衡时,Y的转化率为______;该反应的化学平衡常数K的表达式是______;
(3)能说明该反应已经达到平衡状态的是______;
a.生成1mol?X的同时,生成2mol?Z?b.容器内气体的压强保持不变
c.v逆(X)=v正(Y)?d.容器内气体的密度保持不变
(4)为使该反应的反应速率增大,且能使平衡向正反应方向移动的是______.
a.平衡后及时分离出Z气体?b.平衡后加入高效催化剂
c.平衡后将各物质的量同时加倍?d.平衡后仅增大X的浓度.
参考答案:(1)由图可知10s内,Z的物质的量变化为1.58mol,故v(Z)=1.58mol2L10s=0.079mol/(L?s ).
故答案为:0.079mol/(L.s );
(2)由图可知,Y的起始物质的量为1mol,平衡时Y的物质的量为0.21mol,参加反应的Y的物质的量为1mol-0.21mol=0.79mol,故Y的转化率为0.79mol1mol×100%=79%;
由图象可以看出,反应中X、Y的物质的量减小,Z的物质的量增多,则X、Y为反应物,Z为生成物,10后X、Y、Z的物质的量不再变化,该反应为可逆反应,且△n(X):△n(Y):△n(Z)=(1.2-0.41)mol:(1-0.21)mol:1.58mol=1:1:2,则反应的化学方程式为:X+Y

2Z,该可逆反应的平衡常数k=c2(Z)c(X)?c(Y).
故答案为:79%;c2(Z)c(X)?c(Y).
(3)a.生成1molX相当于消耗2molZ,同时生成2molZ,说明到达平衡,故a正确;
b.该反应气体的物质的量不发生变化,容器内气体的压强自始至终保持不变,压强不变不能说明到达平衡,故b错误;
c.v逆(X)=v正(Y)说明不能物质表示正逆速率之比等于化学计量数之比1:1,说明反应到达平衡,故c正确;
d.反应混合物都是气体,气体的总质量不变,容器的容积一定,容器内气体的密度自始至终保持不变,故密度保持不变不能说明反应到达平衡,故d错误.
故选:ac.
(4)a.平衡后及时分离出Z气体,瞬间逆反应速率减小,正反应速率不变,平衡向正反应进行,随后反应混合物各组分的浓度降低,速率减小,故a错误;
b.平衡后加入高效催化剂,同等程度增大正、逆反应速率,平衡不移动,故b错误;
c.平衡后将各物质的量同时加倍,反应混合物的浓度增大,反应速率增大;该反应气体的物质的量不发生变化压强增大,平衡不移动,故c错误.
d.平衡后仅增大X的浓度,瞬间正反应速率增大,逆反应速率不变,平衡向正反应进行,随后生成物的浓度增大,逆反应速速率增大,故d正确.
故选:d.
本题解析:
本题难度:一般
3、简答题 合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H1=+206.1kJ/mol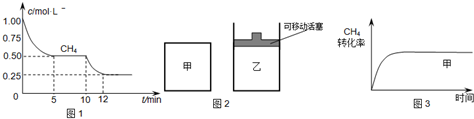
请回答下列问题:
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应中处于平衡状态的时间为______;10min时,改变的外界条件可能是______.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)反应CO(g)+H2O(g)?CO2(g)+H2(g)800℃时,反应的化学平衡常数K=1.0.
①某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2
0.5mol
8.5mol
2.0mol
2.0mol
|
此时反应中正、逆反应速率的关系式是______(填代号).
a.v(正)>v(逆)b.v(正)<v(逆)c.v(正)=v(逆)d.无法判断
②800℃时,向体积为2L的密闭容器中充入2molCO和4molH2O,求达到平衡时CO的转化率.
参考答案:(1)由图可知,由图可知,在5~10分钟、12分钟后,甲烷浓度不变,是平衡状态;10min时甲烷的浓度继续减小,该反应向正反应方向移动,而该反应为吸热反应,则升高温度符合题意,
故答案为:5~10分钟、12分钟后;升高温度;
(2)甲、乙两容器中分别充入等物质的量的CH4和CO2,且甲、乙两容器初始容积相等,由图可知,甲的体积不变,乙的压强不变,则假定甲不变,乙中发生CH4+CO2?2CO+2H2,其体积增大,则相当于压强减小,化学平衡向正反应方向移动,乙容器中CH4的转化率增大,但压强小,反应速率减慢,则达到平衡的时间变长,则乙中CH4的转化率随时间变化的图象为:
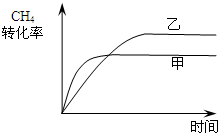 , ,
故答案为: ; ;
(3)由表格中的数据可知,气体的体积相同,则物质的量与浓度成正比,Qc=2.0×2.02.0×8.5<K=1.0,该反应向正反应方向移动,则正反应速率大于逆反应速率,即选a,
故答案为:a;
②800℃时,反应的化学平衡常数K=1.0,向体积为2L的密闭容器中充入2mol CO和4mol H2O,设参加反应的CO为xmol;
CO(g)+H2O(g)?CO2(g)+H2(g)
起始量(mol):2 4 0 0
转化量(mol):x x x x
平衡量(mol):2-x 4-x xx
K=c(CO2)c(H2)c(CO)c(H2O)=x2?x22-x2?4-x2=1,
所以x=43mol,
所以平衡时CO的转化率为:43mol2mol×100%=66.7%,
答:达到平衡时CO的转化率66.7%.
本题解析:
本题难度:简单
4、填空题 接触法制硫酸工艺中,其主反应在450℃并有催化剂存在下进行:
 ? ?
(1)该反应所用的催化剂是____________(填写化合物名称),该反应450℃时的平衡常数________500℃时的平衡常数(填“大于”、“小于”或“等于”)。
(2)能说明上述反应处于平衡状态的是________。
a.
b.容器中气体的平均分子量不随时间而变化
c.容器中气体的密度不随时间而变化
d.容器中气体的分子总数不随时间而变化
(3)在一个固定容积为5L的密闭容器中充入0.20 mol SO2和0.10molO2,半分钟后达到平衡,测得容器中含SO3 0.18mol,则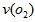 =_________mol・L-1・min-1,若继续通入0.20mol SO2和0.10mol O2,则平衡_________移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,_______mol =_________mol・L-1・min-1,若继续通入0.20mol SO2和0.10mol O2,则平衡_________移动(填“向正反应方向”、“向逆反应方向” 或“不”),再次达到平衡后,_______mol
<n(SO3)<_______mol
参考答案:(1)五氧化二钒(V2O5);大于
(2)bd
(3)0.036;向正反应方向;0.36;0.40
本题解析:
本题难度:一般
5、选择题 T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g).反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的转化率与时间的关系如图2所示.则下列结论正确的是( )
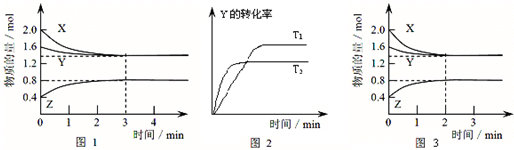
A.容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g)
B.反应进行的前3?min内,用X表示的反应速率?v(X)=0.3mol/(L?min)
C.保持其他条件不变,升高温度,反应的化学平衡常数K减小
D.若改变反应条件,使反应进程如图3所示,则改变的条件是增大压强
参考答案:A
本题解析:
本题难度:简单
| 