1、填空题 根据下列各题所给出的数据,可分别求出其“溶质的质量分数”或“溶质的物质的量
浓度”,试判断并求解。
(1)设NA表示阿伏加德罗常数的数值,若某氢氧化钠溶液V L中含有N个OH-,则可求出此溶液中______________________为__________________。
(2)已知某氢氧化钠溶液中Na+与H2O的个数之比为1∶a,则可求出此溶液中________为________。
(3)已知标准状况下1体积水能溶解500体积的氯化氢,则可求出标准状况下氯化氢饱和溶液中__________为________。
(4)已知将100 mL氯化铝的水溶液加热蒸干灼烧,可得到白色固体b g,则可求出原氯化铝溶液中________为________。
参考答案:(1)溶质的物质的量浓度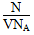 mol/L
mol/L
(2)溶质的质量分数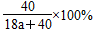
(3)溶质的质量分数 44.9%
(4)溶质的物质的量浓度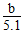 mol/L
mol/L
本题解析:(1)n=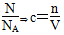 。
。
(2)1∶a?m(NaOH)∶m(H2O)?w=m(NaOH)∶[m(NaOH)+m(H2O)]。
(3)V(HCl)?m(HCl)?w=m(HCl)∶[m(HCl)+m(H2O)]。
(4)b g Al2O3?n(AlCl3)?c。
本题难度:一般
2、选择题 设NA代表阿伏加德罗常数的值,下列叙述不正确的是:
A.标准状况下,NO和O2各11.2L混合,所得混合气体的分子总数为0.75NA
B.常温常压下,Na2O2与足量H2O反应,共生成1molO2,转移电子的数目为2 NA
C.常温常压下,0.l NA个Al与足量氢氧化钠溶液反应生成的H2体积大于3.36 L
D.4.4g CO2所含有的成键电子数约为0.8NA
参考答案:C
本题解析:2NO+O2=2NO2,11.2L一氧化氮和11.2L氧气混合后生成二氧化氮11.2L同时氧气过量5.6L,但二氧化氮与四氧化二氮存在平衡:2NO2 N2O4,所以混合气体体积应介于11.2L~16.8L之间,A错误;2Na2O2+2H2O=4NaOH+O2↑反应中过氧化钠既是氧化剂又是还原剂,每生成1mol氧气转移电子数2mol,B错误;2Al+2NaOH+2H2O=2NaAlO2+3H2↑反应中1mol铝参加反应转移电子数3mol,常温常压下1mol气体体积大于22.4L,C正确;二氧化碳分子中碳原子最外层4个电子与氧原子最外层4个电子形成两个碳碳双键,成键电子数为8,D正确。A
N2O4,所以混合气体体积应介于11.2L~16.8L之间,A错误;2Na2O2+2H2O=4NaOH+O2↑反应中过氧化钠既是氧化剂又是还原剂,每生成1mol氧气转移电子数2mol,B错误;2Al+2NaOH+2H2O=2NaAlO2+3H2↑反应中1mol铝参加反应转移电子数3mol,常温常压下1mol气体体积大于22.4L,C正确;二氧化碳分子中碳原子最外层4个电子与氧原子最外层4个电子形成两个碳碳双键,成键电子数为8,D正确。A
点评:常温常压下,22.4L气体物质的量小于1mol。
本题难度:一般
3、填空题 (8分)下列物质中,物质的量最大的是 ,含分子个数最多的是 ,含原子个数最多的是 ,质量最大的是 。(填字母)
A 6g氢气 B 0.5mol CO2 C 1.204×1024个氯化氢分子 D、147g硫酸
E、92g乙醇(C2H5OH) F、4℃9 mL水
参考答案:A;A;E;D.
本题解析:
试题分析:A、6g H2的物质的量为6/2=3mol,B、0.5mol CO2,C、HCl的物质的量为1.204x1024/6.02x1023=2mol,D、147g H2SO4的物质的量为147/98=1.5mol,E、92g乙醇的物质的量=92/46=2mol,F、水的质量为9mL×1g/mL=9g,水的物质的量为9/18=0.5mol;物质的量最大的是6g氢气,根据N=nNA可知,物质的量越大,含有分子数目越多,故含有分子个数最多的是6g H2;氢气中含有原子为3mol×2=6mol,二氧化碳中含有原子为0.5mol×3=1.5mol,HCl中含有原子为2mol×2=4mol,硫酸中含有原子为1.5mol×7=10.5mol,乙醇中含有原子物质的量=2mol×9=18mol,水中含有原子为0.5mol×3=1.5mol,故含有原子最多的是:92g 乙醇;氢气的质量6g,CO2的质量为0.5mol×44g/mol=22g,HCl的质量为2mol×34g/mol=68g,硫酸的质量147g,乙醇的质量为92g,水的质量为为9mL×1g/mL=9g,故质量最大的是:147g 硫酸,
考点:考查物质的量的相关计算
本题难度:一般
4、选择题 下列关于摩尔的说法中,正确的是
A.是物质的量
B.是一个物理量
C.是一种物理量的单位
D.是摩尔质量