1、填空题 氮化硅(Si3N4)是一种优良的高温结构陶瓷,在工业生产和科技领域有重要用途。
I.工业上有多种方法来制备氮氦化硅,常见的方法有:
方法一?直接氦化法:在1300~1400℃时,高纯粉状硅与纯氦气化合,其反应方程式为
?
方法二?化学气相沉积法:在高温条件下利用四氯化硅气体、纯氦气、氢气反应生成氦化硅和HCl,与方法一相比,用此法制得的氦化硅纯度较高,其原因是?。
方法三? Si(NH?2)4热分解法:先用四氯化硅与氨气反应生成Si(NH?2)4和一种气体
?(填分子式);然后使Si(NH2)4受热分解,分解后的另一种产物的分子式为?。
II.(1)氨化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氨化硅与氢氟酸反应生成四氟化硅和一种铵盐,此盐中存在的化学键类型有?。
(2)已知:25℃,101kPa条件下的热化学方程式:
3Si(s)+2N2(g)==Si3N4(s)?△H=―750.2kJ/mol
Si(s)+2Cl2(g)==SiCl4(g)?△H=―609.6kJ/mol
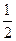 H2(g)+
H2(g)+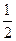 Cl2(g)==HCl(g) △H=―92.3kJ/mol
Cl2(g)==HCl(g) △H=―92.3kJ/mol
请写出四氯化硅气体与氮气、氢气反应的热化学方程式:
?。
III.工业上制取高纯硅和四氯化硅的生产流程如下:
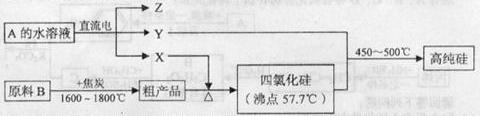
已知:X,高纯硅、原料B的主要成分都可与Z反应,Y与X在光照或点燃条件下可反应,Z的焰色呈黄色。
(1)原料B的主要成分是?。
(2)写出焦炭与原料B中的主要成分反应的化学方程式:?。
(3)上述生产流程中电解A的水溶液时,阳极材料能否用Cu??(填“能”或“不能”)。
写出Cu为阳极电解A的水溶液开始一段时间阴阳极的电极方程式:
阳极:?;阴极:?。
2、选择题 下面关于硅的叙述中,正确的是( )
A.硅的非金属性比碳强,只有在高温下才能跟氢气起化合反应
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位
C.硅的化学性质不活泼,在自然界中可以以游离态存在
D.硅在电子工业中,是重要的半导体材料
3、选择题 普通玻璃的主要成分是:
①Na2SiO3?②CaCO3?③CaSiO3?④SiO2?⑤Na2CO3?⑥CaO
A.①③⑥
B.②③④
C.①③④
D.③④⑤
4、选择题 汉代器物上的颜料“汉紫”至今尚没有发现其自然存在的记载。20世纪80年代科学家进行超导材料研究时,偶然发现其成分为紫色的硅酸铜钡(化学式:BaCuSi2Ox,Cu为+2价),下列有关“汉紫”的说法中不正确的是( )。
A.用盐的形式表示:BaSiO3・CuSiO3
B.用氧化物形式表示:BaO・CuO・2SiO2
C.易溶于强酸、强碱
D.性质稳定,不易褪色
5、选择题 CS2(二硫化碳)无色液体,沸点?46.5℃。储存时,在容器内可用水封盖表面。储存于阴凉、通风的库房,远离火种、热源,库温不宜超过30℃。应与氧化剂、胺类、碱金属、食用化学品分开存放,切忌混储。采用防爆型照明、通风设施。在工业上最重要的用途是制造粘胶纤维。下列说法不正确的是
①属易燃易爆的危险品;②有毒,易水解;③是良好的有机溶剂;
④有氧化性;⑤能与H2S生成H2CS3;⑥能与钠反应但产物中有Na2CO3。
[? ]
A.①④?
B.②③⑥?
C.①④⑤?
D.②⑥