1��ѡ���� ���и������ʣ���һ���Լ����������
A.FeC12��AgNO3��Na2CO3��Na2SO3
B.NaNO3��A1C13��NaCl��MgC12
C.������ϩ�����Ȼ�̼���Ҵ�
D.��NH4)2SO4��NH4Cl��Na2SO4��NaCl
�ο��𰸣�B
���������A ������һ���Լ�������û�������FeC12���а�ɫ��������AgNO3������ɫ��ζ�������ɵ���Na2CO3������ɫ��ζ���������ɵ���Na2SO3
B ������һ���Լ�����
C ����ˮ�������𣬼���ˮ֮���ϲ�ʳȺ�ɫ���DZ�����ɫ���Ǽ�ϩ���²��dzȺ�ɫ�������Ȼ�̼�����ֲ�ĺ����Ҵ���
D ���������������𣬼��а�ɫ���������д̼�����ζ������������ǣ�NH4)2SO4��ֻ�д̼�����ζ�������������NH4Cl��ֻ�а�ɫ�������ɵ���Na2SO4�����������NaCl
��ѡB��
�����Ѷȣ�һ��
2��ѡ���� ���г�ȥ������ѡ�õ��Լ�����ȫ��ȷ���ǣ�?��
A����ȥNaCl��Һ�е�����I2�� ����ˮ�Ҵ�����ȡ��Һ
B���� CO2�е�����HCl��ͨ�뱥��Na2CO3��Һ��ϴ��
C����ȥFeCl2��Һ�е�����FeCl3������������м����ַ�Ӧ����
D����ȥNaHCO3�����е�����Na2CO3����������
�ο��𰸣�C
���������A���Ҵ���ˮ���ܣ�����������ȡˮ��Һ�е�I2������B��Na2CO3��ҺҲ������CO2������C��Fe�ܰ�����FeCl3��ԭΪFeCl2����ȷ��D���������ղ��ܳ�ȥNa2CO3����ʹNaHCO3�ֽ⣬����
�����Ѷȣ�һ��
3��ѡ���� ����ʵ���У�����ȡ�ķ��뷽�����Ӧԭ������ȷ���ǣ�������
| ѡ�� | Ŀ�� | ���뷽�� | ԭ��
A
ʹ��CCl4��ȡ��ˮ�еĵ�
��ȡ��Һ
����CCl4�е��ܽ�Ƚϴ�
B
���������������Ҵ�
��Һ
�����������Ҵ����ܶȲ�ͬ
C
��ȥKNO3�����л��ӵ�NaCl
�ؽᾧ
NaCl��ˮ�е��ܽ�Ⱥܴ�
D
��ȥ�����е�����
����
���������ѵķе����ϴ�
|
A��A
B��B
C��C
D��D
�ο��𰸣�A���ⲻ������ˮ�����������Ȼ�̼����ʹ��CCl4��ȡ��ˮ�еĵ⣬��ȡ���Һ���ɷ��룬��A��ȷ��
B�������������Ҵ����ֲ㣬�������÷�Һ�����룬����������B����
C��NaCl���ܽ�����¶�Ӱ�첻������ص��ܽ�����¶�Ӱ������ȥKNO3�����л��ӵ�NaCl��Ӧ�ܽ����ȴ�ȱ�����Һ���ᾧ���룬��C����
D�����������ѻ��ܣ������߷е㲻ͬ�����ȥ�����е����ѣ��������ɳ��ӣ���D��ȷ��
��ѡAD��
���������
�����Ѷȣ���
4������� ���������û�������������������ų��ķ�������Ҫ��ѧ�ɷ�ΪSiO2Լ45%��Fe2O3Լ40%��Al2O3Լ10%��MgOԼ5%��Ŀǰ�ҹ��Ѿ��ڼ�����ȡ��ͻ�ơ������������з�������ֳɷֲ��������á������̺�����������£�
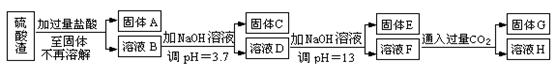
�����ϵ�֪��
��������
| �ܶȻ�(Ksp)
| pHֵ
|
��ʼ����
| ��ȫ����
|
Mg(OH)2
| 5.6��10��12
| 9.3
| 10.8
|
Fe(OH)3
| 2.8��10��16
| 2.7
| 3.7
|
Al(OH)3
| 1.3��10��33
| 3.7
| 4.7
|
?
��ش��������⣺
��1��д������A�Ļ�ѧʽΪ?��
��2����Ҫ�ⶨ��Һ��pH�Ƿ�ﵽ3.7������ʵ����Ʒ�п�ѡ�õ���?��
A��ʯ����Һ? B���㷺pH��ֽ? C������pH��ֽ? D��pH��
��3������������ӷ�Ӧ����ʽ
����ҺD���ɹ���E?��?����ҺF���ɹ���G?��
��4��Ҫ������C������E����G��ת��Ϊ��Ӧ���ȶ����������е�ʵ�����Ϊ?��
��5������������Һ����ı仯���������ҺH��c��Mg2����=?��
�ο��𰸣���1��SiO2��2�֣�
��2��CD��2�֣�
��3��Mg2++2OH�D=Mg(OH)2����2�֣���? AlO2�D+CO2+2H2O=Al(OH)3��+HCO3�D��2�֣�
��4�����Ȼ���»����գ�2�֣�
��5��5.6��10�D10mol/L��2�֣���λ��1�֣�
�����������1����һ���мӹ������ᣬFe2O3��Al2O3��MgO�����ᷴӦ�ܽ⣬SiO2���ܹ��˿ɵã���2��A��ֻ���ж���Һ������ԣ�����B���㷺pH��ֽ ֻ�ܾ�ȷ��������������pH��ֽ ��pH�ƶ����ܾ�ȷ��С�����һλ����ࣻ��4�������еõ��Ĺ���Ϊ��������������տɵ������
��5����ҺHΪ����pH=13��õ�����Һ��c(OH��)=0.1 mol/L
c(Mg2+)= Ksp��c2(OH��)= 5.6��10��12��0.12=5.6��10�D10mol/L
�����Ѷȣ�һ��
5������� (14��) Mg(ClO3)2����������������ݼ��ȣ���ͼΪ�Ʊ�����Mg(ClO3)2��6H2O�ķ�����
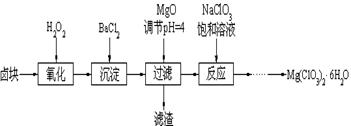
��֪��1��±����Ҫ�ɷ�ΪMgCl2��6H2O������MgSO4��FeCl2�����ʡ�
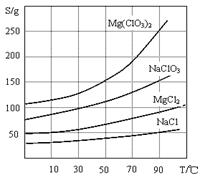
2�����ֻ�������ܽ��(S)���¶�(T)�仯��������ͼ��
��1������BaCl2��Ŀ���dz�_________������жϸ������ѳ���_____________________��
��2������NaClO3������Һ�ᷢ����Ӧ��MgCl2��2NaClO3==Mg(ClO3)2��2NaCl���������ø÷�Ӧ������ܽ��ͼ����ȡMg(ClO3)2��6H2O��ʵ�鲽������Ϊ��
��ȡ��������NaClO3������Һ��ַ�Ӧ��������Ũ������?������ȴ�ᾧ��
�ݹ��ˡ�ϴ�ӣ����Mg(ClO3)2��6H2O���塣
��Ʒ��Mg(ClO3)2��6H2O�����IJⶨ��
����1��ȷ����3.50g��Ʒ�ܽⶨ�ݳ�100mL��Һ��
����2��ȡ10mL��õ���Һ����ƿ�У�����10mLϡ�����20mL1.000mol/L��FeSO4��Һ���ȡ�
����3����ȴ�����£���0.100mol/L K2Cr2O7��Һ�ζ����յ㣬�˹����з�Ӧ�����ӷ���ʽΪ��
Cr2O72����6Fe2����14H��==2Cr3����6Fe3����7H2O��
����4��������2��3�ظ����Σ�ƽ������K2Cr2O7��Һ15.00mL��
��3��д������2����������Ӧ�����ӷ���ʽ?��
��4������3�����ζ�ǰ�ñ�Һ��ϴ�ζ��ܣ��ᵼ�����ս��?���ƫ����ƫС�����䡱����
��5����Ʒ��Mg(ClO3) 2��6H2O����������Ϊ?(������������λС��) ��
�ο��𰸣���14�֣�(1)?SO42-?��2�֣� ?
���ã�ȡ�ϲ���Һ����BaCl2�����ް�ɫ��������SO42-�ѳ�����ȫ��2�֣�
��2�����ȹ��� ��2�֣�
��3��6H++ClO3-+6Fe2+==6Fe3++Cl-+3H2O ��3�֣�
��4������ ��2�֣�
��5�� 78.31%?��3�֣�
�����������1������BaCl2��Ŀ���dz�ȥSO42-������������������ӽ�ϳ����ᱵ���������˳�ȥ������SO42-�Ƿ�����ķ����Ǿ��ã�ȡ�ϲ���Һ����BaCl2�����ް�ɫ��������SO42-�ѳ�����ȫ��
��2��Mg(ClO3)2���ܽ�����¶ȱ仯Ӱ����¶ȸ�ʱ�ܽ�Ƚϴ��¶ȵ�ʱ�ܽ�Ƚ�С��������Ҫ���ȹ��˳�ȥ�Ȼ��ƣ�
��3������2����������Ӧ��ClO3-��Fe2+�����������µ�������ԭ��Ӧ�����������Ӻ������ӡ�ˮ�����ӷ���ʽΪ6H++ClO3-+6Fe2+==6Fe3++Cl-+3H2O��
��4���ζ����ڼ����Һǰ�����ñ�Һ��ϴ���������ս�����䣻
��5����������K2Cr2O7��Һ15.00mL�ɼ���δ��ClO3-�������������ӵ����ʵ�����0.015L��0.1mol/L��6=0.009mol����ClO3-�������������ӵ����ʵ�����0.02L��1mol/L-0.009mol=0.011mol����100mL��Һ��ClO3-�����ʵ�����0.011mol��1/6��10=0.11/6mol,����Ʒ��Mg(ClO3) 2��6H2O������Ϊ0.11/6mol/2��299g/mol=2.741g�����Բ�Ʒ��Mg(ClO3) 2��6H2O����������Ϊ2.741g/3.5g��100%=78.31%.
�����Ѷȣ�����