1��ѡ���� ���в���Ҫ�õ������������
A�����ά
B�������оƬ
C��ʯӢ�ӱ�
D���������
�ο��𰸣�B
�����������
�����Ѷȣ�һ��
2��ѡ���� ����ɫ��ѧ�����У�����״̬�Ƿ�Ӧ���е�ԭ��ȫ��ת��Ϊ���ƵõIJ����ԭ��������Ϊ100%������CH3C�TCH�ϳ�CH2�TC��CH3��COOCH3�Ĺ����У���ʹԭ�������ʴﵽ��ߣ�����Ҫ��������Ӧ���У�������
A��CO2��H2O
B��CO��CH3OH
C��CH3OH��H2
D��H2��CO2
�ο��𰸣������ڡ���ɫ��ѧ�������У�ԭ��������Ϊ100%�������ɵIJ�ƷCH2�TC��CH3��COOCH3��ԭ��֮��Ԫ�������ԭ����Ŀ����ȫ��ͬ����ԭ���غ㣮���������и�ԭ�Ӹ�����ȥ��Ӧ���и�ԭ�Ӹ����õ�һЩԭ�ӣ�����Ⱦ�ķ�Ӧ;����������ʼ̬ʵ����ȾԤ���������ն������Ŀ�ѧ�ֶΣ�������ͨ����ѧת����ȡ�����ʵĹ������ѳ�������˸���ԭ�ϣ�����������̺�ĩ�˵IJ�ֵΪC2H4O2������ѡ���Ӧ����ԭ����֮��ΪC2H4O2��ֻ��B��
��CH3C�TCH����Ȳ���ϳ�CH2�TC��CH3��COOCH3��2-����ϩ���������Ҫ��һ��C3H4���ӱ��һ��C5H8O2���ӣ�����������2��Cԭ�ӡ�4��Hԭ�ӡ�2��Oԭ�ӣ���ԭ���������������C��H��O��ԭ�Ӹ�����Ϊ1��2��1��
A��CO2��H2O���������ʷ���������ԭ�Ӳ����������Ҳ������ʹC��H��O��ԭ�Ӹ�����Ϊ1��2��1����A����
B��CO��CH3OH����������������շ��Ӹ�����1��1��ϣ���C��H��O��ԭ�Ӹ�����Ϊ1��2��1����B��ȷ��
C��CH3OH��H2���������ʷ���������ԭ�Ӳ���������϶�����ʹC��H��O��ԭ�Ӹ�����Ϊ1��2��1����C����
D��H2��CO2�����������ʷ���������ԭ�Ӳ����������Ҳ������ʹC��H��O��ԭ�Ӹ�����Ϊ1��2��1����D����
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ��ѧ����Դ������������������Դ���õ�������أ�����˵����ȷ���ǣ�������
A��Ϊ���ũ����IJ�����������Ӧ����ʹ�û��ʺ�ũҩ
B����ɫ��ѧ�ĺ�����Ӧ�û�ѧԭ���Ի�����Ⱦ��������
C��ʵ�ֻ�ʯȼ��������ã������迪������Դ
D�������ǷŴ��ط�����Դ��Ӧ�����������
�ο��𰸣�D
���������
�����Ѷȣ�һ��
4������� ��10�֣�����������һ��������Ư�������㷺Ӧ����ϴ�·ۡ�Ư�ۡ�ϴ�Ӽ��С�����ɰ(��Ҫ��ΪNa2B4O7)Ϊԭ�������������ƾ������Ҫ�������£�
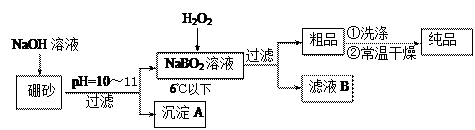
��1����Na2B4O7��NaOH��Ӧ��NaBO2�����ӷ���ʽΪ? ��?��
��2������A�к���������������þ���ʣ�Ϊ�˷����������þ���ڳ����мӹ������ᣬ���˵õ���Mg2+����Һ��������Һ�����ʹMg2+�γ�������þ�����Ӽ�ǰ��Һ��c(Mg2+)��0.056 mol?L-1����ô�������Һ��pH��? ��?ʱ���ſ�ʼ���ֳ�����[��֪25����Mg(OH)2��Ksp��5.6��10��12]
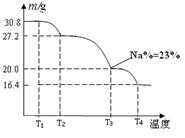
��3����֪��Ʒ�������ƾ����и�Ԫ�ص����ʵ�����Ϊ��n(Na):n(B): n(H) :n(O)="1:" 1: n: 7�����ƵõĴ�Ʒ��Ʒ��70�����ϼ��Ƚ���ʧȥ�ᾧˮ����ô�Ʒ�������¶ȵı仯��ͼ��ʾ����T3ʱ���þ���Ļ�ѧʽΪ___��___������д������̣�
��4������Ӧ�¶ȿ��Ʋ��������õĹ������ƾ� ���н�����NaBO2 �����Ʒ���Ƶ���������?��?���� �����ߡ��������͡����䡱����
���н�����NaBO2 �����Ʒ���Ƶ���������?��?���� �����ߡ��������͡����䡱����
�ο��𰸣���ÿ��2�֣���10�֣���1��B4O 72- + 2OH- = 4BO2- + H2O ��2�֣�
72- + 2OH- = 4BO2- + H2O ��2�֣�
��2��pH ��9?��2�֣�
��3��NaBO3��H2O ����ѧʽ2�֣�����2�֣���4�֣�
������̣�T3ʱ��nNa=��20.0g��23%��/23g.mol-1="0.2mol?" ��1�֣�
��30.8g��Ʒ�У�nNa:nB:nH:nO=0.2:0.2:0.2n:1.4
��0.2��23+0.2��11+0.2n+1.4��16=30.8
���n="8?" ��ԭ����Ϊ��NaBO3��4H2O?(1��)
��һ������T3ʱ���þ�������Ԫ�ص���������������ᾧˮ��ĿΪ1 ��
����T3ʱ���þ���Ļ�ѧʽΪNaBO3��H2O?��2�֣�
��4������?��2�֣�
�����������
�����Ѷȣ�һ��
5������� ������ũҵ������ռ����Ҫλ�á�������ũѧר���ձ���Ϊ���������������ز��������£�ũ����ʩ�û��ʿ�����40����60�����ϳɰ���ҵ�����ṩ�����ĵ��ʣ��������������ʳ��������ķdz���Ҫ�Ļ�ѧ��ҵ��
��1���ڹ�ҵ�ϳɰ��ķ�Ӧ�У����ڸ÷�Ӧ�ڳ��³�ѹ�£����ü������ܾ��죬Ҫʵ�ֹ�ҵ���dz����ѣ����ѧ��Ϊ�˽����˲�и��Ŭ���������ȴ��¶Ⱥ�ѹǿ���֣��¶����߶����ѧ��Ӧ����?�����������������أ�������ѹǿ�����ѧ��Ӧ����?�����������������أ�����ѧ������Ȼѡ���˺��ʵ��¶Ⱥ�ѹǿ����Ч�����ѣ�����Ͷ�빤ҵ���������¹���ѧ�ҹ�����Fritz Haber��1868��1934��ͨ��Ŭ������ʹ�ú��ʴ�������������ڽ����������⣬ʵ���˺ϳɰ��Ĺ�ҵ������������Ϊ�÷�Ӧ�ܹ�ҵ�������Ĺؼ���?
��2���ϳɰ�����Ҫ���˹��̵����������˹��̵��⣬������Ȼ�̵�������̵�������Ȼ�̵���һ�ַ�ʽ�������Ͽ��ø�ѹ������ģ����һ���̣�װ����ͼ��ʾ��
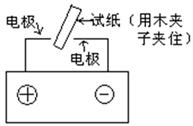
ʵ�鿪ʼ���Կ���ʪ�����ɫʯ����ֽ���ɫ�������ԭ���÷�Ӧ�Ļ�ѧ����ʽ��ʾ��
?
??
?
�ο��𰸣���1��������?������?ʹ�ú��ʵĴ���
��2��N2 + O2 �� 2NO
2NO + O2 �� 2NO2
3NO2 + H2O �� 2HNO3 + NO��
�����������
�����Ѷȣ���