1������� �������ʣ���ʯī�����������HNO3�����ڵ����ᱵ��NaOH����ޱ������NH3��H2O�൨��
��1����������ǿ����ʵ��� �����ţ���
��2�����ڢۢ�������������ˮ�����pH��ͬ����Һ����������Һ�����ʵ���Ũ������Ϊc1��c2��c3�����������ʵ���Ũ���ɴ�С��˳��Ϊ ��ȡ�������pH������������Һ���ֱ��������п�ۣ���Ӧ�����зų�H2����������Ϊv1��v2��v3�����С��ϵΪ ��
��3��ij�¶�ʱ�����0.01mol��L-1��NaOH��pH=13�����¶���ˮ�����ӻ�����Kw = ��
�ο��𰸣���8�֣���1���ۢܢݢ� ��2��c3,>c2>c1�� v1=v2<v3��3��1��10-15
�����������1������Һ����ȫ����ĵ����Ϊǿ����ʣ���Ϊ�ۢܢݢࣻ��2��������������ˮ�������ᣬ�Ƕ�Ԫǿ�ᣬ������һԪǿ�ᣬ����Ϊ���ᣬ����pH��ͬ����Һ�����ʵ���Ũ��Ϊc3,>c2>c1�����ŷ�Ӧ�Ľ��У�����ĵ���ƽ�������ƶ�������v1=v2<v3����3��pH="13" ��c(H+)=10-13mol��L-1 , Kw ="0.01" mol��L-1��10-13mol��L-1=10-15��
���㣺����ʣ�����ʵĵ��롢��Һ��pH
�����Ѷȣ�һ��
2��ѡ���� ������������ˮ������뷽��ʽ��ȷ���ǣ�������
A��NaHCO3=Na++H++CO32-
B����NH4��2SO4=NH4++SO42-
C��NH4Cl=NH4++Cl-
D��Ba��OH��2=Ba2++OH2-
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� �й�����������Һ��˵���У���ȷ���ǣ�������
��Һ�٣�0.2mo1?L-1?CH3COONa��Һ��
��Һ�ڣ�0.1mo1?L-1H2SO4��Һ��
A����ͬ�¶��£���Һ��ˮ�ĵ���̶ȣ���Һ�٣���Һ��
B����ˮϡ����Һ�٣���Һ��
c(CH3COOH)?c(OH-)
c(CH3COO-)
|
���
C������������Һ�ٺ���Һ�ڣ�������Һ��c��CH3COO-��+2c��SO42-��=c��Na+��
D��25��ʱ������Һ���еμ���Һ����pH=7����Һ��c��Na+����c��SO42-��
�ο��𰸣�A����Һ����ǿ����������Һ�����������ˮ���Լ��ԣ��ٽ�ˮ�ĵ��룺��Һ��������Һ����ˮ�ĵ������������ã���ͬ�¶��£���Һ��ˮ�ĵ���̶ȣ���Һ�٣���Һ�ڣ���A����
B����ˮϡ�ʹٽ���������ӵ�ˮ�⣬�����ı�ˮ��ƽ�ⳣ������Һ��c(CH3COOH)?c(OH-)c(CH3COO-)���䣬��B����
C����Һ�ٺ���Һ�ڵ�������ǡ�÷�Ӧ���ɴ���������ƣ���Һ�����ԣ���Һ�д��ڵ���غ�����жϣ�[Na+]+[H+]=[OH-]+[CH3COO-]+2[SO42-]����c[CH3COO-]+2[SO42-]=[Na+]�õ�[H+]=[OH-]����������Һ�����ԣ���C����
D��25��ʱ����Һ��Ϻ�PH=7����Һ�����ԣ���Һ�д��ڵ���غ㣻[Na+]+[H+]=[OH-]+[CH3COO-]+2[SO42-]��[H+]=[OH-]��c[CH3COO-]+2[SO42-]=[Na+]����Һ��c��Na+����c��SO42-������D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
4������� д������������ˮ��Һ�еĵ��뷽��ʽ
�Ȼ�ͭ______
������______
̼������______
��������______��
�ο��𰸣��Ȼ�ͭ��ǿ����ʣ�����ʱ����������ƶ���ͭ���Ӻ������ӣ�CuCl2=Cu2++2Cl-��
������ǿ����ʣ�����ʱ����������ƶ��������Ӻ���������ӣ�Fe2��SO4��3=2Fe3++3SO42-��
̼��������ˮ�е���������Ӻ�̼��������ӣ����뷽��ʽΪNaHCO3�TNa++HCO3-��
NaHSO4��ǿ����ʣ�NaHSO4��ˮ�е���������Ӻ���������Ӻ������ӣ�NaHSO4�TNa++H++SO42-��
�ʴ�Ϊ��CuCl2=Cu2++2Cl-��Fe2��SO4��3=2Fe3++3SO42-��NaHCO3�TNa++HCO3��NaHSO4�TNa++H++SO42-��
���������
�����Ѷȣ���
5��ѡ���� ����ͼʾ���Ӧ������������ǣ� ��
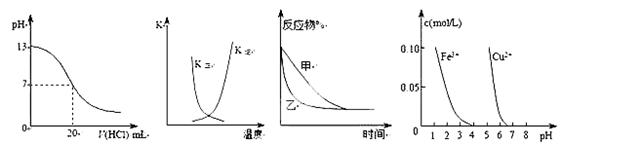
�� �� �� ��
A��ͼ�ٱ�ʾ25��ʱ����0.1 mol��L��1����ζ�20 mL 0.1 mol��L��1NaOH��Һ����Һ��pH�����������ı仯
B��ͼ�������߱�ʾ��Ӧ2A(g) + B(g) 2C(g) ��H > 0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
2C(g) ��H > 0�������淴Ӧ��ƽ�ⳣ��K���¶ȵı仯
C��ͼ�۱�ʾѹǿ�Կ��淴Ӧ2A(g)+2B(g)  3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
3C(g)+D(s)��Ӱ�죬�ҵ�ѹǿ�ȼ�ѹǿ��
D����ͼ������ȥCuSO4��Һ�е�Fe3+������Һ�м�������CuO��pH��4���ҡ�